
【题目】化学上常用AG表示溶液中的酸碱度,AG=lg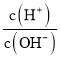 。25℃时,用0.100mol·L-1的NaOH溶液滴定20.00mL0.100mol·L-1HNO2溶液,AG与所加NaOH溶液的体积(V)关系如图所示,下列说法正确的是( )
。25℃时,用0.100mol·L-1的NaOH溶液滴定20.00mL0.100mol·L-1HNO2溶液,AG与所加NaOH溶液的体积(V)关系如图所示,下列说法正确的是( )
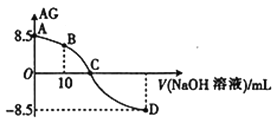
A. D点溶液中的pH=11.25
B. B点溶液中存在c(H+)-c(OH-)=c(NO2-)-c(HNO2)
C. C点时,加入NaOH溶液的体积为20.00mL
D. 25℃时,HNO2的电离平衡常数Ka=1.0×10-5.5
【答案】A
【解析】A、D点溶液中的AG=-8.5,即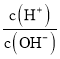 =10-8.5,又Kw= c(H+)× c(OH-)=10-14,求得c(H+)=10-11.25 mol·L-1,则pH=11.25,故A正确;B、B点溶液中存在的溶质为等物质的量的HNO2和NaNO2,由电荷守恒得c(H+)+ c(Na+)=c(OH-)+c(NO2-),其物料守恒为2c(Na+)=c(HNO2)+ c(NO2-),联立即得2c(H+)-2c(OH-)=c(NO2-)-c(HNO2),故B错误;C、C点溶液呈中性,因反应的生成物NaNO2水解使溶液呈碱性,所以C点时加入NaOH溶液的体积为略小于20.00mL,则C错误;D、由图象可知0.100mol·L-1HNO2溶液的AG=8.5,即
=10-8.5,又Kw= c(H+)× c(OH-)=10-14,求得c(H+)=10-11.25 mol·L-1,则pH=11.25,故A正确;B、B点溶液中存在的溶质为等物质的量的HNO2和NaNO2,由电荷守恒得c(H+)+ c(Na+)=c(OH-)+c(NO2-),其物料守恒为2c(Na+)=c(HNO2)+ c(NO2-),联立即得2c(H+)-2c(OH-)=c(NO2-)-c(HNO2),故B错误;C、C点溶液呈中性,因反应的生成物NaNO2水解使溶液呈碱性,所以C点时加入NaOH溶液的体积为略小于20.00mL,则C错误;D、由图象可知0.100mol·L-1HNO2溶液的AG=8.5,即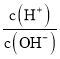 =108.5,又Kw= c(H+)×c(OH-)=10-14,c(H+)=10-2.75mol·L-1,所以Ka=
=108.5,又Kw= c(H+)×c(OH-)=10-14,c(H+)=10-2.75mol·L-1,所以Ka=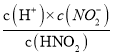 =
=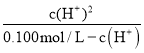 ≈1.0×10-4.5,故D错误。本题正确答案为A。
≈1.0×10-4.5,故D错误。本题正确答案为A。


 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案科目:高中化学 来源: 题型:
【题目】pH=1的两种酸溶液A、B各1 mL,分别加水稀释到1000 mL,其pH与溶液体积的关系如图,下列说法正确的是( )

①若a<4,则A、B都是弱酸
②稀释后,A酸溶液的酸性比B酸溶液强
③若a=4,则A是强酸,B是弱酸
④A、B两种酸溶液的物质的量浓度一定相等
A. ①④ B. ②③ C. ①③ D. ②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(本题共8分)现有部分元素的性质与原子(或分子)结构如下表:
元素编号 | 元素性质与原子(或分子)结构 |
T | 最外层电子数是次外层电子数的3倍 |
X | 常温下单质为双原子分子,分子中含有3对共用电子对 |
Y | M层比K层少1个电子 |
Z | 第三周期元素的简单离子中半径最小 |
(1)写出元素T的原子结构示意图 。
(2)元素Y与元素Z相比,金属性较强的是________(用元素符号表示),下列表述中能证明这一事实的是________(填序号)。
a.Y单质的熔点比Z单质低
b.Y的化合价比Z低
c.Y单质与水反应比Z单质剧烈
d.Y最高价氧化物的水化物的碱性比Z强
(3)T、X、Y、Z中有两种元素能形成既有离子键又有非极性共价键的化合物,写出该化合物的电子式:_____ _________。
(4)元素T和氢元素可形成一种18电子的化合物Q,元素X与氢元素也能按原子个数比为1∶2形成一种18电子化合物W,Q与W发生氧化还原反应,生成X单质和T的另一种氢化物,写出该反应的化学方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下列各装置图的叙述中正确的是( )
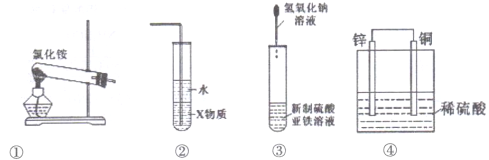
A. 装置①可用于实验室用制取氨气
B. 装置②中X若为四氯化碳,可用于吸收氨气
C. 装置③可用于制备氢氧化亚铁并观察其颜色
D. 装置④是原电池,锌电极为负极,发生还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌铜原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过,下列有关叙述正确的是( )
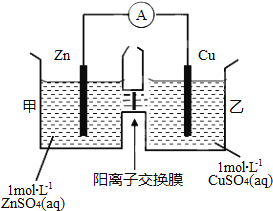
A. 铜电极上发生氧化反应
B. 电池工作一段时间后,甲池的c(SO42-)减小
C. 电池工作一段时间后,乙池溶液的总质量增加
D. 阴阳离子离子分别通过交换膜向负极和正极移动,保持溶液中电荷平衡
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】微生物电池是指在微生物的作用下将化学能转化为电能的装置,其工作原理如图所示。下列有关微生物电池的说法错误的是 ( )

A. 正极反应中有CO2生成
B. 微生物促进了反应中电子的转移
C. 质子通过交换膜从负极区移向正极区
D. 电池总反应为C6H12O6+6O2===6CO2+6H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】细胞内含有多种有机物,下图表示细胞内有机物的元素组成和功能的关系,其中A、B代表元素,Ⅰ、Ⅱ、Ⅲ、Ⅳ是生物大分子,x、Y、Z、P分别为构成生物大分子的基本单位。请回答下列问题:

(1)I在小麦种子中主要是指____________,I在动物细胞中主要是指____________。若物质R与I具有相似功能,并且在动物、植物细胞均含有,不仅含能量多而且体积较小,则物质R是____________。
(2)与Y相比,Z特有的成分有____________。
(3)P通过____________反应形成Ⅳ,此过程生成的H2O中H原子来自P的____________(基团)。
(4)Ⅳ结构不同的原因是____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有HCl、H2O、NH3三种物质,它们都含有1mol氢原子,则三种物质的物质的量之比为( )
A.1∶1∶1B.6∶3∶2C.3∶2∶1D.1∶2∶3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com