
 .
.分析 (1)①焦炭在高温下可以置换二氧化硅中的硅;
②根据熔沸点的不同实现物质分离的方法为蒸馏或分馏;
(2)在铁制品腐蚀的电化学腐蚀中,金属铁作负极发生氧化反应;
(3)氧化铝是两性氧化物,既能和强酸反应又能和强碱反应,均放出氢气;
(4)AlFe(OH)nCl6-n中各元素的化合价代数和为0,丙烯腈(CH2=CH-CN)中的双键能发生加聚反应;
(5)铜、银合金与足量的某浓度的硝酸反应,硝酸所起作用为酸性和氧化性,起酸性作用的硝酸生成硝酸铜、硝酸银,起氧化性作用的硝酸被还原为氮的氧化物(无法确定具体物质),氮的氧化物与氧气混合通入水中,反应又生成硝酸,根据氮元素守衡,该硝酸的量恰好等于起氧化性作用的硝酸的量.所以有铜、银合金失去的电子总数等于氧气获得的电子总数.利用铜、银合金失去的电子总数等于氧气获得的电子总数以及铜、银合金总质量为14g,列方程求解.
解答 解:(1)①工业上用焦炭在高温下置换二氧化硅中的硅来制备粗硅,方程式为:SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑,
故答案为:SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑;
②SiHCl3(沸点33.0℃)、SiCl4(沸点57.6℃)、HCl(沸点-84.7℃),他们的沸点不同,根据沸点的不同实现物质分离的方法为蒸馏或分馏,故答案为:蒸馏或分馏;
(2)在铁制品的电化学腐蚀中,金属铁作负极发生氧化反应,电极反应为:Fe-2e-→Fe2+,
故答案为:Fe-2e-→Fe2+;
(3)氧化铝是两性氧化物,既能和强酸反应又能和强碱反应,
故答案为:Al2O3+6H+═2Al3++3H2O、Al2O3+2OH-+3H2O=2[Al(OH)4]-;
(4)化合物中铝元素显+3价,氢氧根为-1价,各元素的化合价代数和为0,故铁元素的化合价为+3价,丙烯腈(CH2=CH-CN)中的双键能发生加聚反应,方程式为: ,故答案为:+3;
,故答案为:+3; ;
;
(5)n(O2)=$\frac{1.12g}{22.4g/mol}$=0.05mol
设Cu、Ag的物质的量分别为x、y,则:
根据质量列方程:x×64g/mol+y×108g/mol=14g
根据电子守恒列方程:2x+1×y=0.05mol×4
解得:x=0.05mol;y=0.1mol
m(Cu)=0.05mol×64g/mol=3.2g,
故答案为:3.2g.
点评 本题是一道有关硅的无机推断题,考查的知识点范围较广,涉及原电池、两性氧化物、高分子材料、氧化还原反应的计算等,题目难度中等.


 智能训练练测考系列答案
智能训练练测考系列答案 计算高手系列答案
计算高手系列答案科目:高中化学 来源: 题型:选择题
| A. | 活化分子间的碰撞一定能发生化学反应 | |
| B. | 升高温度时,化学反应速率加快,主要原因是反应物分子的能量增加,活化分子百分数增大,有效碰撞次数增多 | |
| C. | 自发进行的反应一定迅速 | |
| D. | 凡是熵增加的过程都是自发过程 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
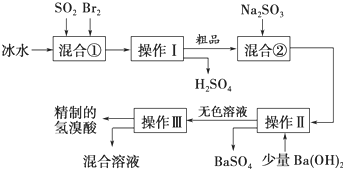
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
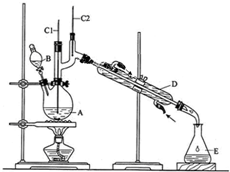
| 沸点/℃ | 密度/g•cm-3 | 水中溶解性 | |
| 正丁醇 | 117.2 | 0.8109 | 微溶 |
| 正丁醛 | 75.7 | 0.8017 | 微溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某实验小组同学为了探究铜与浓硫酸的反应,进行了如下系列实验:
某实验小组同学为了探究铜与浓硫酸的反应,进行了如下系列实验:查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如图:
醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如图:| 相对分子质量 | 密度/(g•cm3) | 沸点/℃ | 溶解性 | |
| 环己醇 | 100 | 0.9618 | 161 | 微溶于水 |
| 环己烯 | 82 | 0.8102 | 83 | 难溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 25℃、101KPa时,16g O2和O3混合气体中含有的原子数为NA | |
| B. | 1 mol NH3中含有的质子数为17NA | |
| C. | 11.2 L O2和N2的混合气体含有的分子数为0.5NA | |
| D. | 金属铁与稀盐酸反应当产生0.1 mol H2时转移电子数为0.3NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com