
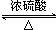 CH3COOC2H5+H2O.
CH3COOC2H5+H2O.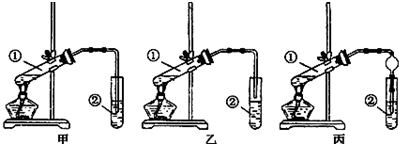
分析 【实验原理】乙酸和乙醇在浓硫酸作用下发生酯化反应,生成乙酸乙酯和水;
【装置设计】酸和乙醇易溶于水,不插入液面下是为了防止倒吸,所以选乙装置;球形干燥管导气的同时也起到防倒吸作用;
【问题讨论】(1)浓硫酸有吸水性,促进该反应向正反应方向移动,浓硫酸能加快反应速率,所以浓硫酸作催化剂和吸水剂;
(2)碳酸钠溶液中的水溶解乙醇,能跟乙酸反应吸收乙酸,便于闻到乙酸乙酯的香味,而乙酸乙酯难溶于饱和碳酸钠溶液;
(3)乙酸乙酯难溶于饱和碳酸钠溶液,所以步骤E试管②中液体分层;
(4)因为乙酸乙酯难溶于饱和碳酸钠溶液,分离互不相溶液体的方法是分液.
解答 解:【实验原理】乙酸和乙醇在浓硫酸作用下发生酯化反应,生成乙酸乙酯和水,化学方程式为CH3COOH+C2H5OH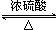 CH3COOC2H5+H2O,
CH3COOC2H5+H2O,
故答案为:CH3COOH+C2H5OH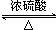 CH3COOC2H5+H2O;
CH3COOC2H5+H2O;
【装置设计】酸和乙醇易溶于水,不插入液面下是为了防止倒吸,所以选乙装置;球形干燥管导气的同时也起到防倒吸作用,
故答案为:乙;防止倒吸;
【问题讨论】(1)浓硫酸有吸水性,促进该反应向正反应方向移动,浓硫酸能加快反应速率,所以浓硫酸作催化剂和吸水剂,所以实验中浓硫酸的作用是:催化、吸水,故答案为:催化、吸水;
(2)碳酸钠溶液中的水溶解乙醇,能跟乙酸反应吸收乙酸,便于闻到乙酸乙酯的香味,而乙酸乙酯难溶于饱和碳酸钠溶液,所以试管2中加入的X试剂为:饱和碳酸钠溶液,故答案为:饱和碳酸钠溶液;
(3)乙酸乙酯难溶于饱和碳酸钠溶液,所以步骤E试管②中观察到的现象是:液体分为两层(有水果味),故答案为:液体分为两层(有水果味);
(4)因为乙酸乙酯难溶于饱和碳酸钠溶液,分离互不相溶液体的方法是分液,所以常用分液分离获得实验中的乙酸乙酯,故答案为:分液.
点评 本题考查制备实验方案的设计,为高频考点,把握乙酸乙酯的制备原理、实验装置的作用、混合物分离提纯方法为解答的关键,侧重分析与实验能力的考查,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
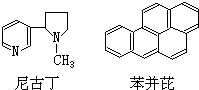 吸烟是人类的一种不良嗜好,也是生活环境中的特殊大气污染源,它对人体健康危害极大,据分析吸烟生成的物质至少有700多种,其中大部分为有毒有害物质.危害最大的物质中有两种是尼古丁和苯并芘,前者的成人致死量约为40~60mg,相当于一包香烟产生的尼古丁的总量;后者是最强的致癌物之一.它们的结构简式分别为:
吸烟是人类的一种不良嗜好,也是生活环境中的特殊大气污染源,它对人体健康危害极大,据分析吸烟生成的物质至少有700多种,其中大部分为有毒有害物质.危害最大的物质中有两种是尼古丁和苯并芘,前者的成人致死量约为40~60mg,相当于一包香烟产生的尼古丁的总量;后者是最强的致癌物之一.它们的结构简式分别为:| A. | 尼古丁的分子式为C10H14N2 | |
| B. | 尼古丁分子中的所有原子都在同一平面上 | |
| C. | 苯并芘的分子式为C20H18 | |
| D. | 苯并芘分子中含有苯环结构单元,是苯的同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 100kg | B. | 160kg | C. | 240kg | D. | 300kg |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaOH+HCl═NaCl+H2O | B. | 2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3 | ||
| C. | SO3+H2O═H2SO4 | D. | NH4HCO3 $\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
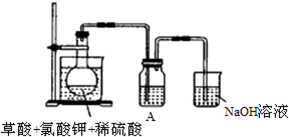
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
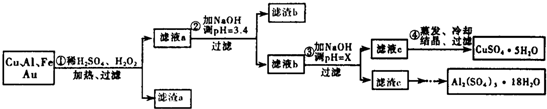
| 沉淀物 | Fe(OH)3 | Al(OH3) | Cu(OH)2 |
| 开始沉淀 | 1.1 | 4.0 | 5.4 |
| 完全沉淀 | 3.2 | 5.2 | 6.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
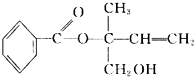
| A. | 有机物M和油脂都含有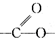 ,两者在酸性或碱性条件下都能发生取代反应 ,两者在酸性或碱性条件下都能发生取代反应 | |
| B. | M在一定条件下能发生加聚反应,不能发生酯化反应 | |
| C. | 在Ni作催化剂的条件下,1 mol M最多只能与1molH2加成 | |
| D. | 不可用酸性高锰酸钾溶液区分苯和M |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com