
某化学兴趣小组按照下列方案进行“由含铁废铝制备硫酸铝晶体”的实验:
步骤1:取一定量含铁废铝,加足量的NaOH溶液,反应完全后过滤。
步骤2:边搅拌边向滤液中滴加稀硫酸至溶液的pH=8~9,静置、过滤、洗涤。
步骤3:将步骤2中得到的固体溶于足量的稀硫酸。
步骤4: 。
请回答以下问题:
(1)上述实验中的过滤操作需要玻璃棒、 等玻璃仪器。
(2)步骤1发生反应的离子方程式为
过滤的目的是__________________________________________。
(3)当步骤2中的溶液pH=8~9时,检验沉淀是否完全的方法是______________。
(4)步骤2中溶液的pH控制较难操作,可改用____________________,发生反应的离子方程式为 。
(5)步骤4的操作为 。
【知识点】铝的重要性质 实验操作 C2 J1 J2
【答案解析】(1)烧杯、漏斗 (2)略,除去铁等不溶于碱的杂质
(3)取上层清液,逐滴加入稀硫酸,若变浑浊则说明沉淀不完全,若不变浑浊则说明沉淀完全
(4)通入足量CO2气体,略
(5)将得到的溶液蒸发浓缩、冷却、结晶、过滤、干燥
解析::(1)过滤操作中需要大小烧杯各一个、漏斗、玻璃棒,因此过滤操作中需要的玻璃仪器有:烧杯、漏斗、玻璃棒;
(2)Al能与氢氧化钠溶液反应生成偏铝酸钠和氢气,化学方程式为:2Al+2NaOH+2H2O═2NaAlO2+3H2↑,
Al能与氢氧化钠溶液反应,铁不能与氢氧化钠溶液反应,通过过滤将杂质铁从溶液中除掉,
(3)检验沉淀是否完全的方法是取上层清液,逐滴加入稀硫酸,若变浑浊则说明沉淀不完全,若不变浑浊则说明沉淀完全。
(4)边搅拌边向滤液中滴加稀硫酸至溶液的pH=8~9,目的是生成氢氧化铝,可利用往偏铝酸钠溶液中通入足量CO2气体的方法,不必控制溶液的PH就可得到最大量的沉淀。
(5)步骤3:将步骤2中得到的固体溶于足量的稀硫酸得到硫酸铝溶液,将得到的溶液蒸发浓缩、冷却、结晶、过滤、干燥得晶体。
【思路点拨】本题考查了铝的重要性质和实验操作,掌握铝能与强碱性溶液反应而铁不与强碱性溶液反应是关键。


 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源: 题型:
下列各组物质中,不属于同分异构体的是( )
A.乙苯和二甲苯
B.CH2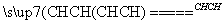 CH2和CH3CCCH3
CH2和CH3CCCH3
C.CH3CH2CH3和CH3(CH2)3CH3
D.CH3CH2OH和CH3OCH3
查看答案和解析>>
科目:高中化学 来源: 题型:
偏二甲肼与N2O4 是常用的火箭推进剂,二者发生如下化学反应:
(CH3)2NNH2 (l )+2N2O4 (l )=2CO2 (g )+3N2 (g )+4H2O (l ) (Ⅰ)
(1)若将反应(Ⅰ)设计成原电池,则正极的电极反应式为
(酸性电解质)。
(2)火箭残骸中常现红棕色气体,原因为:N2O4 (g) 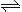 2NO2 (g) (Ⅱ)
2NO2 (g) (Ⅱ)
当温度升高时,气体颜色变深,则反应(Ⅱ)为 (填“吸热”或“放热”)反应。
(3)一定温度下,反应(Ⅱ)的焓变为ΔH。现将1 mol N2O4 充入一恒压密闭容器中,
下列示意图正确且能说明反应达到平衡状态的是________.
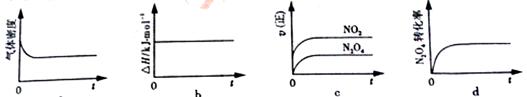
若在相同温度下,上述反应改在体积为1L的恒容密闭容器中进行,平衡常数________(填“增大”“不变”或“减小”),反应3s后NO2的物质的量为0.6mol,则0~3s内的平均反应速率v(N2O4)=________mol·L-1·s-1。
(4)NO2可用氨水吸收生成NH4NO3 。25℃时,将amol NH4NO3溶于水,溶液显酸性,原因是 (用离子方程式表示)。向该溶液滴加bL氨水后溶液呈中性,则滴加氨水的过程中的水的电离平衡将______(填“正向”“不”或
“逆向”)移动,所滴加氨水的浓度为_______mol·L-1。(NH3·H2O的电离平衡常数
Kb=2×10—5 mol·L-1)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验、现象及相关结论均正确的是( )
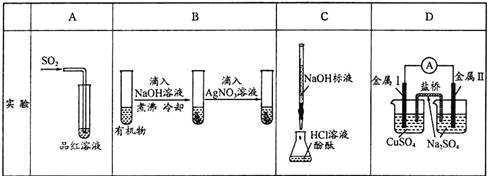
| 现象 | 品红褪色 | 最后试管有浅黄色沉淀 | 最后一滴溶液使酚酞由无色变为粉红色,且30秒不复原 | 盐桥左端从 无色逐渐变为 蓝色 |
| 结论 |
氧化性 | 有机物中含 有溴原子 | 滴定达到终点 | 金属II比I活泼 |
查看答案和解析>>
科目:高中化学 来源: 题型:
有关下列物质说法不正确的是( )
A.Na、Mg、Fe等金属在一定条件下与水反应都生成H2和对应的碱
B.相同温度下,等物质的量浓度的Na2CO3和NaHCO3溶液pH:Na2CO3 > NaHCO3
C.将两支蘸有浓盐酸和浓氨水的玻璃棒相互靠近有大量白烟产生
D.HCl、NH3、CO2都极易溶于水,都可用水作吸收剂做喷泉实验
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式正确的是
A. 铝溶于NaOH溶液:Al+2OH—=AlO2—+H2↑
B. 铜溶于稀硝酸:3Cu+ 8H+ +2NO3—=3Cu2+ +2NO↑ + 4H2O
C. 碳酸镁中滴加稀盐酸:CO32—+2H+ =CO2↑ + H2O
D. 稀硫酸中滴加氢氧化钡溶液:H++ OH—=H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
A由Al2O3、Fe3O4、Al、Cu中的某几种粉末混合而成,该混合物成分的分析方案如下图所示。
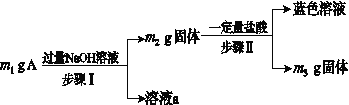
下列分析错误的是( )
A.当m1>m2时,溶液a中的阴离子只有1种
B.生成蓝色溶液的离子方程式为Cu+2Fe3+===Cu2++2Fe2+
C.要确定混合物中是否含有Al,可取A加入适量稀盐酸
D.当m2-m3=2.96 g时,Fe3O4的质量至少为2.32 g
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验过程中,始终无明显现象的是( )
A.Cl2通入FeSO4溶液中 B.CO2通入Ca(OH)2溶液中
C.将AlCl3溶液滴入 NaOH 溶液中 D.SO2通入BaCl2溶液中
查看答案和解析>>
科目:高中化学 来源: 题型:
能源、环境与人类生活和社会发展密切相关,研究它们的综合利用有重要意义。
(1)氧化—还原法消除氮氧化物的转化如下: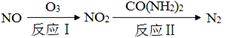
①反应Ⅰ为:NO+O3=NO2+O2,生成11.2 L O2(标准状况)时,转移电子的物质的量是 mol。
②反应Ⅱ中,当n(NO2)∶n[CO(NH2)2]=3∶2时,反应的化学方程式是 。
(2)硝化法是一种古老的生产硫酸的方法,同时实现了氮氧化物的循环转化,主要反应为:NO2(g)+SO2(g) SO3(g)+NO(g) △H=-41.8 kJ·mol-1已知:2SO2(g)+O2(g)
SO3(g)+NO(g) △H=-41.8 kJ·mol-1已知:2SO2(g)+O2(g) 2SO3(g) △H=-196.6 kJ·mol-1,写出NO和O2反应生成NO2的热化学方程式 。
2SO3(g) △H=-196.6 kJ·mol-1,写出NO和O2反应生成NO2的热化学方程式 。
某化学兴趣小组构想将NO转化为HNO3,装置如下图一,电极为多孔惰性材料。则负极的电极反应式是 。
(4)将燃煤废气中的CO2转化为二甲醚的反应原理为:2CO2(g)+6H2(g) CH3OCH3(g)+3H2O(g);
CH3OCH3(g)+3H2O(g);
①该反应平衡常数表达式为K= 。
②已知在某压强下,该反应在不同温度、不同投料比时,CO2的转化率如右图二所示。该反应的ΔH________(填“>”、“<”或“=”)0。
(5)合成气CO和H2在一定条件下能发生如下反应:CO(g) +2H2(g) CH3OH(g) △H<0。在容积均为VL的I、Ⅱ、Ⅲ三个相同密闭容器中分别充入amol CO和2a mol H2,三个容器的反应温度分别为T1、T2、T3且恒定不变,在其他条件相同的情况下,实验测得反应均进行到t min时CO的体积分数如图三所示,此时I、Ⅱ、Ⅲ三个容器中一定达到化学平衡状态的是 ;若三个容器内的反应都达到化学平衡时,CO转化率最大的反应温度是 。
CH3OH(g) △H<0。在容积均为VL的I、Ⅱ、Ⅲ三个相同密闭容器中分别充入amol CO和2a mol H2,三个容器的反应温度分别为T1、T2、T3且恒定不变,在其他条件相同的情况下,实验测得反应均进行到t min时CO的体积分数如图三所示,此时I、Ⅱ、Ⅲ三个容器中一定达到化学平衡状态的是 ;若三个容器内的反应都达到化学平衡时,CO转化率最大的反应温度是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com