
食盐中的抗结剂是亚铁氰化钾,其化学式为K4[Fe(CN)6]·3H2O。42.2 g K4[Fe(CN)6]·3H2O样品受热脱水过程的热重曲线(样品质量随温度的变化曲线)如下图所示。
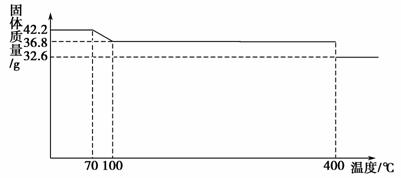
试回答下列问题:
(1) 试确定150 ℃时固体物质的化学式_________________________________
_________ ______________
______________ __________________________________________。
__________________________________________。
(2) 查阅资料知:虽然亚铁氰化钾自身毒性很低,但其水溶液与酸反应放出极毒的氰化氢(HCN)气体;亚铁氰化钾加热至一定温度时能分解产生氰化钾(KCN)。据此判断,烹饪食品时应注意的问题为_______________________________________________________________________________________
________________________________________________________________。
(3) 在25 ℃时,将a mol·L-1的KCN溶液与0.01 mol·L-1的盐酸等体积混合,反应达到平衡时,测得溶液pH=7,则KCN溶液的物质的量浓度a________0.01 mol·L-1(填“>”、“<”或“=”);用含a的代数式表示HCN的电离常数Ka=__________________________________________
________________________________________________________________。
(4)在Fe2+、Fe3+的催化作用下,可实现2SO2+ O2+2H2O===2H2SO4的转化。已知,含SO2的废气通入含Fe2+、Fe3+的溶液中时,其中一个反应的离子方程式为4Fe2++O2+4H+===4Fe3++2H2O,则另一个反应的离子方程式为________________________________________________________________________。
O2+2H2O===2H2SO4的转化。已知,含SO2的废气通入含Fe2+、Fe3+的溶液中时,其中一个反应的离子方程式为4Fe2++O2+4H+===4Fe3++2H2O,则另一个反应的离子方程式为________________________________________________________________________。
上述转化的重要意义在于___________________________________________
________________________________________________________________。
(5)已知Fe(OH)3的溶度积常数Ksp=1.1×10-36。室温时在FeCl3溶液中滴加NaOH溶液,当溶液pH为3时,通过计算说明Fe3+是否沉淀完全____________________________________________________________________________________________________________________________________。
(提示:当某离子浓度小于10-5 mol·L-1时可以认为该离子沉淀完全)
解析 (1)对于加热失去结晶水的研究,注意开始时质量变化为失去水的质量:
K4[Fe(CN)6]·3H2O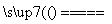 K4[Fe(CN)6]·xH2O+(3-x)H2O
K4[Fe(CN)6]·xH2O+(3-x)H2O
1 3-x
0.1 mol 0.3 mol
x=0
则150 ℃时固体 物质的化学式为K4[Fe(CN)6]。
物质的化学式为K4[Fe(CN)6]。
(2)为防止有毒的HCN和KCN生成,应避免与酸性物质接触和控制烹饪温度。
(3)由于KCN+HCl===HCN+KCl,当反应后pH=7,则溶液中有过量的KCN,故a>0.01 mol·L-1
由溶液中电荷守恒得:c(K+)+c(H+)=c(OH-)+c(CN-)+c(Cl-),又因为pH=7,则c(H+)=c(OH-),故c(K+)=c(CN-)+c(Cl-)=0.5a mol·L-1
由物料守恒得:c(K+)=c(CN-)+c(HCN),则c(HCN)=c(Cl-)=0.005 mol·L-1c(CN-)=(0.5a-0.005)mol·L-1
平衡常数K=c(CN-)·c(H+)/c(HCN)=(0.5a-0.005)×10-7/0.005 mol·L-1。
答案 (1)K4[Fe(CN)6]
(2)避免与醋等酸性物质一起烹饪;控制烹饪温度不超过400 ℃
(3)> (0.5a-0.005)×10-7/0.005 mol·L-1
(4)2Fe3++SO2+2H2O===2Fe2++SO42-+4H+ 变废为宝,消除污染 (5)c(Fe3+)=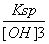 =1.1×10-3 mol·L-1>1×10-5 mol·L-1,故Fe3+没有沉淀完全
=1.1×10-3 mol·L-1>1×10-5 mol·L-1,故Fe3+没有沉淀完全


 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案科目:高中化学 来源: 题型:
按下图电解NaCl的饱和溶液,写出该电解池中发生反应的总反应方程式:________。

将充分电解后所得溶液逐滴加入到酚酞试液中,观察到的现象是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
无论是从在国民经济中的地位来看,还是从科学发展的角度来看,硅都发挥着重要的作用。
(1)人类使用硅酸盐产品(陶瓷等)的历史已经快一万年了,但在1823年才获得单质硅,瑞典化学家贝采尼乌斯用金属钾还原SiF4获得单质硅,写出化学方程式_______________ 。
(2)由于制取方法和条件的不同,得到的单质硅形态不同,其性质也不同。
①用铝热法还原氟硅酸钾制得较纯净的晶体硅:4Al+3K2SiF63Si+2K AlF4+2K2AlF5,关于该反应的说法正确的是________(填序号)。
AlF4+2K2AlF5,关于该反应的说法正确的是________(填序号)。
A.Al是还原剂 B .氧化产物只有KAlF4
.氧化产物只有KAlF4
C.每转移6NA电子,得到42 g Si D.Al元素在KAlF4和K2AlF5中化合价不同
②用白砂子与镁粉混合在高温条件下得到无定形硅,反应的化学方程式为___________ 。
(3)在野外,为了迅速得到氢气,用硅粉与干燥的Ca(OH)2和NaOH混合,并加强热,即可迅速得到H2、Na2SiO3、CaO。这种混合物叫做生氢剂。请写出该反应的化学方程式___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:25 ℃时,Ksp[Mg(OH)2]=5.61×10-12,Ksp(MgF2)=7.42×10-11。下列说法正确的是( )。
A.25 ℃时,饱和Mg(OH)2溶液与饱和MgF2溶液相比,前者的c(Mg2+)大
B.25 ℃时,在Mg(OH)2的悬浊液加入少量的NH4Cl固体,c(Mg2+)增大
C.25 ℃时,Mg(OH)2固体在20 mL 0.01 mol·L-1氨水中的Ksp比在20 mL 0.01 mol·L-1NH4Cl溶液中的Ksp小
D.25 ℃时,在Mg(OH)2的悬浊液中加入NaF溶液后,Mg(OH)2不可能转化成为MgF2
查看答案和解析>>
科目:高中化学 来源: 题型:
能在溶液中大量共存的一组离子是 ( )。
A.NH4+、Ag+、PO43-、Cl-
B.Fe3+、H+、I-、HCO3-
C.K+、Na+、NO3-、MnO4-
D.Al3+、Mg2+、SO42-、CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
某无色溶液中含有K+、Cl-、OH-、SO32-、SO42-,为检验溶液中所含的各种阴离子,限用的试剂有:盐酸、硝酸、硝酸银溶液、硝酸钡溶液和溴水。检验其中OH-的实验方法从略,检验其他阴离子的过程如下图所示。

(1)图中试剂①~⑤溶质的化学式分别是:
①__________,②__________,③__________,④__________
⑤_____ _____。
_____。
(2)图中现象a、b、c表明检验出的离子分别是:
a__________、b__________、c__________。
(3)白色沉淀A加试剂②反应的离子方程式是____________________________
__________________。
(4)无色溶液C加试剂③的主要目的是_________________________________
______________________________。
(5)白色沉淀A若加试剂③而不加试剂②,对实验的影响是___________________________________________
 ________。
________。
(6)气体E通入试剂④发生反应的离子方程式是__________________________
____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列醇中,不能氧化成与其碳原子数相同的醛的是( )
A、2,3-二甲基-2-丁醇
B、2,2-二甲基-1-丁醇
CH3 H
C、 CH3- C- C-OH
CH3 H
D、CH3-CH2-CH-CH2-OH
CH3
查看答案和解析>>
科目:高中化学 来源: 题型:
甲、乙、丙三种溶液各含有一种X-(X-为Cl-、Br-、I-)离子。向甲中加淀粉溶液和氯水,则溶液变为橙色,再加丙溶液,颜色无明显变化。则甲、乙、丙依次含有( )
A.Br-、Cl-、I- B.I-、Br-、Cl- C.Br-、I-、Cl- D.Cl-、I-、Br-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com