
| ||
| ||


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
 美国每日科学网站4月2日文章报道:美国梅奥诊所的研究人员发现绿茶含有有助于消灭血癌细胞的成分.这项研究利用实验室培养的细胞显示,绿茶中称作“表没食子儿茶素没食子酸酯”(EGCG)的成分通过干扰血癌细胞生存所需的信号传递,能使血癌(白血病)中癌细胞自杀性死亡.另据华夏经纬网2004年2月25日报道,日本科学家发现绿茶中的EGCG能中和脂肪酸合成酵素(Fatty acid synthase简称:FAS),从而能阻止艾滋病毒扩散.已知一个碳原子连接四个不同的原子或原子团叫手性碳原子,且EGCG的结构式如图,有关EGCG的说法不正确的是( )
美国每日科学网站4月2日文章报道:美国梅奥诊所的研究人员发现绿茶含有有助于消灭血癌细胞的成分.这项研究利用实验室培养的细胞显示,绿茶中称作“表没食子儿茶素没食子酸酯”(EGCG)的成分通过干扰血癌细胞生存所需的信号传递,能使血癌(白血病)中癌细胞自杀性死亡.另据华夏经纬网2004年2月25日报道,日本科学家发现绿茶中的EGCG能中和脂肪酸合成酵素(Fatty acid synthase简称:FAS),从而能阻止艾滋病毒扩散.已知一个碳原子连接四个不同的原子或原子团叫手性碳原子,且EGCG的结构式如图,有关EGCG的说法不正确的是( )| A、EGCG分子中含有两个手性碳原子 |
| B、EGCG遇FeCl3溶液能发生显色反应 |
| C、1molEGCG最多可与含10mol氢氧化钠的溶液完全作用 |
| D、EGCG在空气中易氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 1866年凯库勒(如图)提出了苯的单、双键交替的正六边形平面结构,解释了苯的部分性质,但还有一些问题尚未解决,它不能解释的事实是( )
1866年凯库勒(如图)提出了苯的单、双键交替的正六边形平面结构,解释了苯的部分性质,但还有一些问题尚未解决,它不能解释的事实是( )| A、苯不能使溴水褪色 |
| B、苯能与H2发生加成反应 |
| C、溴苯没有同分异构体 |
| D、苯能与HNO3发生取代反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加入铝粉能放出氢气的溶液:Na+、Cl-、SO42-、Fe3+ |
| B、使紫色石蕊试液变红的溶液:Fe2+、Mg2+、NO3-、Cl- |
| C、c(OH-)=10-12 mol?L-1的溶液:K+、Ba2+、Cl-、Br- |
| D、在含有大量AlO2-的溶液中:NH4+、Na+、Cl-、H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
 A、B、C、D、E五种物质都含同一种元素,C为一种淡黄色的固体化合物.它们按如图所示的关系相互转化,已知A为单质.分别写出有关反应的化学方程式.
A、B、C、D、E五种物质都含同一种元素,C为一种淡黄色的固体化合物.它们按如图所示的关系相互转化,已知A为单质.分别写出有关反应的化学方程式.查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
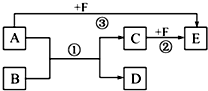 已知:A、B、C、D、E、F是中学化学教材中六种常见的物质,它们之间有如图所示的相互转化关系(反应条件及部分产物未标出).请回答下列问题:
已知:A、B、C、D、E、F是中学化学教材中六种常见的物质,它们之间有如图所示的相互转化关系(反应条件及部分产物未标出).请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
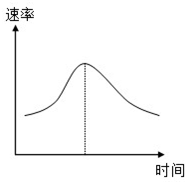 氯酸钾和亚硫酸氢钠发生氧化还原反应生成Cl(-1价)和S(+6价)的速率如图曲线所示,已知ClO3-的氧化性随c(H+)的增大而增强,有关方程式为:ClO3-+3HSO3-?Cl-+3H++3SO42-
氯酸钾和亚硫酸氢钠发生氧化还原反应生成Cl(-1价)和S(+6价)的速率如图曲线所示,已知ClO3-的氧化性随c(H+)的增大而增强,有关方程式为:ClO3-+3HSO3-?Cl-+3H++3SO42-查看答案和解析>>
科目:高中化学 来源: 题型:
| A、稀释浓硫酸时,应将浓硫酸沿玻璃棒注入盛有水的烧杯,同时边加边搅拌. |
| B、某溶液加入硝酸酸化的氯化钡溶液产生白色沉淀,则溶液中一定含有SO42-离子 |
| C、制作印刷电路板的过程中常用氯化铁溶液与铜反应 |
| D、某气体通入品红溶液能使品红褪色,则该气体不一定是SO2气体. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com