
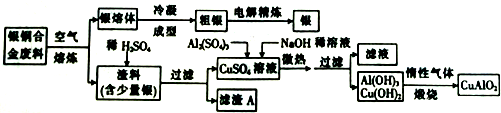
分析 由工艺流程图可知,废料在空气中熔炼时,Cu被氧化,滤渣中含有CuO及少量Ag,向滤渣中加入硫酸进行酸浸,CuO与硫酸反应,过滤得到硫酸铜溶液(含有硫酸),滤渣A为Ag;向滤液中加入硫酸铝、氢氧化钠,得到氢氧化铝、氢氧化铜,灼烧中会得到CuO、Al2O3,二者反应得到CuAlO2,银熔体冷却成型得到粗银,通过电解精炼得到银,
(1)废料在空气中熔炼时,Cu被氧化,滤渣中含有CuO及少量Ag,元素化合价升高的被氧化得到氧化产物;
(2)向滤渣中加入硫酸进行酸浸,CuO与硫酸反应,过滤得到硫酸铜溶液(含有硫酸),滤渣A为Ag;由上述分析可知,CuO、Al2O3反应得到CuAlO2,由电荷守恒可知,O元素化合价升高,有氧气生成;
(3)向CuSO4溶液中加入Al2(SO4)3和NaOH稀溶液,其中NaOH稀溶液的作用是沉淀铝离子和铜离子;
(4)电解精炼银的原理是利用电解池中粗银做阳极,精银作阴极,含银离子的电解质溶液做电解质溶液;
(5)若产品CuAlO2能溶于浓硝酸发生氧化还原反应,亚铜离子被氧化为铜离子,硝酸钡还原为二氧化氮,结合原子守恒配平书写化学方程式,若有1 mol CuAlO2参与反应,生成气体的体积(标准状况下)小于22.4L,可能是二氧化氮转化为四氧化二氮,或生成一氧化氮气体;
解答 解:由工艺流程图可知,废料在空气中熔炼时,Cu被氧化,滤渣中含有CuO及少量Ag,向滤渣中加入硫酸进行酸浸,CuO与硫酸反应,过滤得到硫酸铜溶液(含有硫酸),滤渣A为Ag;向滤液中加入硫酸铝、氢氧化钠,得到氢氧化铝、氢氧化铜,灼烧中会得到CuO、Al2O3,二者反应得到CuAlO2,银熔体冷却成型得到粗银,通过电解精炼得到银,
(1)废料在空气中熔炼时,Cu被氧化,滤渣中含有CuO及少量Ag,元素化合价升高的被氧化得到氧化产物CuO,
故答案为:CuO;
(2)向滤渣中加入硫酸进行酸浸,CuO与硫酸反应,过滤得到硫酸铜溶液(含有硫酸),滤渣A为Ag;等物质的量的Al(OH)3与Cu(OH)2在惰性气体中煅烧时生成氧化铜、氧化铝,依据生成产物有CuAlO2,反应前Cu为+2价,反应后为+1,化合价降低1,Al化合价没有变化,所以氧元素的化合价升高,生成氧气,反应前氧为-2价,反应后为0,化合价升高2,两者的最小公倍数是2,再根据原子守恒得:4CuO+2Al2O3=4CuAlO2+O2↑,
故答案为:Ag;O2;
(3)向CuSO4溶液中加入Al2(SO4)3和NaOH稀溶液,其中NaOH稀溶液的作用是沉淀铝离子和铜离子生成氢氧化铝和氢氧化铜沉淀,
故答案为:使铝离子和铜离子沉淀完全;
(4)电解精炼银的原理是利用电解池中粗银做阳极,精银作阴极,含银离子的电解质溶液做电解质溶液,选择硝酸银溶液做电解质溶液,
故答案为:AgNO3溶液;粗银;
(5)若产品CuAlO2能溶于浓硝酸发生氧化还原反应,亚铜离子被氧化为铜离子,硝酸钡还原为二氧化氮,结合电子守恒、原子守恒配平书写化学方程式为:CuAlO2+6HNO3(浓)=Cu(NO3)2+Al(NO3)3+NO2↑+3H2O,可能是生成的二氧化氮转化为四氧化二氮,随硝酸浓度减小变稀后会生成一氧化氮都可能导致生成气体的体积(标准状况下)小于22.4L,
故答案为:CuAlO2+6HNO3(浓)=Cu(NO3)2+Al(NO3)3+NO2↑+3H2O;二氧化氮转化为四氧化二氮;生成了一氧化氮;
点评 本题考查了物质分离提纯的过程分析,主要是物质性质、电解原理、氧化还原反应电子守恒、等知识点的理解应用,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 氯分子的电子式: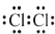 | B. | 氯离子(Cl-)的结构示意图: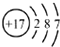 | ||
| C. | 中子数为20的氯原子: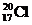 | D. | 氯乙烯分子的结构简式:H3C-CH2Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 ClO2是一种高效水处理剂,某实验小组用如图所示装置制取并收集ClO2.已知:
ClO2是一种高效水处理剂,某实验小组用如图所示装置制取并收集ClO2.已知:| 信息 | 内容 |
| ① | ClO2为黄绿色气体,极易溶于水,熔点为-59℃,沸点为11℃,具有强氧化性 |
| ② | ClO2易爆炸,若用惰性气体等稀释,则爆炸的可能性大降低 |
| ③ | HClO4、HClO2均是强酸,HClO4为无色透明液体,沸点为90℃;HClO2很不稳定,容易分解 |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应速率:乙>甲 | B. | 平衡时C的体积分数:乙>甲 | ||
| C. | 平衡时C的转化率:乙>甲 | D. | 平衡时A的物质的量:甲>乙 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3COO- | B. | SO32- | C. | CO32- | D. | HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 4N2(g)+6H2O(g);△H
4N2(g)+6H2O(g);△H| 反应 | △H(kJ•mol-1) | 平衡常数(K) |
| 4NH3 (g)+5O2 (g)?4NO (g)+6H2O (g) | -905.5 | 1.1×1026mol•L-1 |
| 4NH3 (g)+4O2 (g)?2N2O (g)+6H2O (g) | -1104.9 | 4.4×1028 |
| 4NH3 (g)+3O2 (g)?2N2 (g)+6H2O (g) | -1269.0 | 7.1×1034L•mol-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com