
| A、c(CH3COO-)>c(Na+) |
| B、c(CH3COOH)>c(CH3COO-) |
| C、2c(H+)=c(CH3COO-)-c(CH3COOH) |
| D、c(CH3COOH)+c(CH3COO-)=0.02mol/L |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①② | B、①③ | C、①④ | D、③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、体系的压强不再改变 |
| B、各组分的浓度不再改变 |
| C、反应速率νA:νB:νC:νD=“m“:n:p:q |
| D、单位时间内m mol A断键发生反应,同时p mol C也断键发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
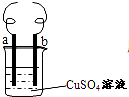 用铁丝(电极a)、铜丝(电极b)和CuSO4溶液可以构成原电池或电解液,如图所示,则下列说法正确的是( )
用铁丝(电极a)、铜丝(电极b)和CuSO4溶液可以构成原电池或电解液,如图所示,则下列说法正确的是( )| A、构成原电池时b极反应式为:Cu2++2e-=Cu |
| B、构成电解池时a极质量一定减少 |
| C、构成电解池时b极质量可能减少也可能增加 |
| D、构成的原电池或电解池工作后,两电极均产生大量气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、分别中和等质量的氢氧化钠,消耗盐酸和醋酸溶液的体积相同 |
| B、分别跟足量的镁完全反应,无法比较两者产生氢气的总量大小 |
| C、滴入2滴甲基橙试液后加入等体积的pH=12的Ba(OH)2,溶液仍呈红色 |
| D、分别加水稀释相同的倍数,盐酸中由水电离出的c(H+)比醋酸溶液大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com