
| A. | SO2和O2 | B. | NO和O2 | C. | H2S和SO2 | D. | NH3和HCl |
 金牌课堂练系列答案
金牌课堂练系列答案 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案科目:高中化学 来源: 题型:选择题
| A. | 氢氧化钠溶液 | B. | 氢氧化钡溶液 | C. | 氨水溶液 | D. | 澄清的石灰水 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④⑥⑦⑧⑨ | B. | ②④⑥⑦⑧⑨ | C. | ①④⑥⑧ | D. | ①②④⑧⑨ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 •
•查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
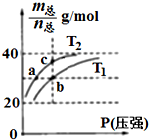 已知(HF)2(g)?2HF(g),△H>0,且平衡体系的总质量[m(总)]与总物质的量[n(总)]之比在不同温度下随压强的变化曲线如图所示.下列说法正确的是( )
已知(HF)2(g)?2HF(g),△H>0,且平衡体系的总质量[m(总)]与总物质的量[n(总)]之比在不同温度下随压强的变化曲线如图所示.下列说法正确的是( )| A. | 温度:T1<T2 | |
| B. | 平衡常数:K(a)=K(b)<K(c) | |
| C. | 反应速率:Vb>Va | |
| D. | 当$\frac{m(总)}{n(总)}$=30g/mol时,n(HF):n(HF)2=2:1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com