
| A. | 明矾净水 | B. | 钢铁生锈 | C. | 海水提溴 | D. | 工业固氮 |
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:高中化学 来源: 题型:解答题
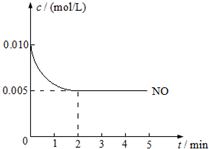 2NO(g)+O2(g)?2NO2(g)△H<0是制造硝酸的重要反应之一.在800℃时,向容积为1L的密闭容器中充入0.010mol NO和0.005molO2,反应过程中NO的浓度随时间变化如图所示:
2NO(g)+O2(g)?2NO2(g)△H<0是制造硝酸的重要反应之一.在800℃时,向容积为1L的密闭容器中充入0.010mol NO和0.005molO2,反应过程中NO的浓度随时间变化如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 1-丁醇 | 冰醋酸 | |
| 密度(g/cm3) | 0.81 | 1.05 |
| 摩尔质量(g/mol) | 74 | 60 |
| A. | 产率:约54.49% | B. | 产率:约42.04% | ||
| C. | 转化率:冰醋酸小于1-丁醇 | D. | 转化率:冰醋酸大于1-丁醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解熔融NaCl制取Na,故电解熔融MgCl2也能制取Mg | |
| B. | Fe与CuSO4溶液反应置换出Cu,故Na也能从CuSO4溶液中置换出Cu | |
| C. | 通常元素的价态越高对应物质的氧化性越强,故HClO4的氧化性强于HClO | |
| D. | CO2和Na2O2反应生成Na2CO3和O2,故SO2和Na2O2反应生成Na2SO3和O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
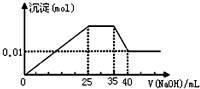 有一未知的无色溶液,只可能含有以下离子中的若干种(忽略由水电离产生的H+、OH-):H+、NH4+、K+、Mg2+、Cu2+、Al3+、NO3-、CO32-,现取样逐滴滴加NaOH溶液,测得沉淀与NaOH溶液的体积关系如图.以下推测错误的是( )
有一未知的无色溶液,只可能含有以下离子中的若干种(忽略由水电离产生的H+、OH-):H+、NH4+、K+、Mg2+、Cu2+、Al3+、NO3-、CO32-,现取样逐滴滴加NaOH溶液,测得沉淀与NaOH溶液的体积关系如图.以下推测错误的是( )| A. | 原溶液一定不存在H+、Cu2+、CO32- | |
| B. | 不能确定原溶液是否含有K+、NO3- | |
| C. | 原溶液中n(Mg2+):n(Al3+):n(NH4+)=1:1:2 | |
| D. | 实验所加的NaOH溶液浓度为2mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 软脂酸(C15H31COOH) | B. | 油酸(C17H33COOH) | ||
| C. | 草酸(HOOC-COOH) | D. | 氨基酸(H2N-CH2COOH) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
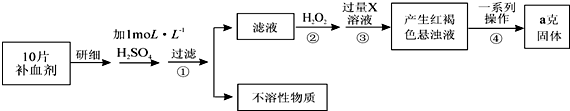
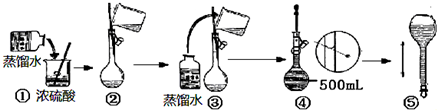
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com