
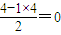 ,为sp3杂化,立体构型为正四面体,故A不选;
,为sp3杂化,立体构型为正四面体,故A不选;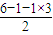 =1,为sp3杂化,立体构型为三角锥型,故B不选;
=1,为sp3杂化,立体构型为三角锥型,故B不选; =1,为sp3杂化,立体构型为三角锥型,故C不选;
=1,为sp3杂化,立体构型为三角锥型,故C不选; ,中心原子为sp2杂化,立体构型为平面三角形,故D选;
,中心原子为sp2杂化,立体构型为平面三角形,故D选;

科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
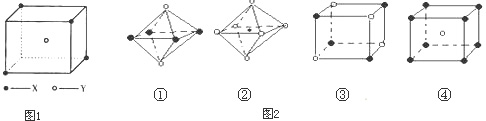
| 3 |
| ||
| 2 |
| 3 |
| ||
| 2 |
| 分子或离子 | H2S | CO32- | PH3 | ClO4-- |
| 空间构型 | V型 V型 |
平面三角形 平面三角形 |
三角锥型 三角锥型 |
正四面体 正四面体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
(10分)(1)(6分)向盛有硫酸铜水溶液的试管里逐渐滴加氨水至过量,观察到的实验现象是: 其反应的离子方程式为: 、
(2)(4分)利用VSEPR理论推测下列分子或离子的空间构型:CO32-和SO32-的空间构型分别为 、和 。其中心原子的杂化方式分别是 和
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com