
| A. | 用碱式滴定管取23.10mL溴水 | |
| B. | 为测定新制氯水的pH,用玻璃棒蘸取液体滴在pH试纸上,与标准比色卡对照即可 | |
| C. | 做蒸馏实验时,在蒸馏烧瓶中应加入沸石,以防暴沸.如果在沸腾前发现忘记加沸石,应立即停止加热,冷却后补加 | |
| D. | 提纯混有少量硝酸钾的氯化钠,应采用在较高温度下制得浓溶液再冷却结晶、过滤、干燥的方法 |
分析 A.溴水具有氧化性,能够氧化碱式滴定管的橡胶管;
B.氯水中的次氯酸能漂白pH试纸;
C.蒸馏操作中需要加入沸石,若在沸腾前发现忘记加沸石,应立即停止加热,冷却后补加,避免发生爆沸现象;
D.氯化钠中混有少量的硝酸钾,不能制得硝酸钾的饱和溶液.
解答 解:A.溴水能够氧化碱式滴定管的橡胶管,应该用酸式滴定管量取,故A错误;
B.氯水具有强氧化性,能漂白pH试纸,不能用pH试纸测定新制氯水的pH值,故B错误;
C.液体加热要加沸石或碎瓷片,引入汽化中心,可防止溶液暴沸,如果加热一段时间后发现忘记加碎瓷片,应该采取停止加热,待溶液冷却后重新添加碎瓷片,该操作合理,故C正确;
D.氯化钠中混有少量的硝酸钾,氯化钠是大量的,制得的饱和溶液中硝酸钾量较少,不能采取降温结晶的方法,故D错误;
故选C.
点评 本题考查了化学实验基本操作方法及评价,题目难度中等,明确正确的操作方法为解答关键,B为易错点,注意氯水具有氧化性的特点,试题培养了学生的分析能力及化学实验能力.


 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案科目:高中化学 来源: 题型:选择题
| A. | 麦芽糖及其水解产物均能发生眼镜反应 | |
| B. | 可用新制Cu(OH)2,鉴别甲酸、乙醛和乙酸 | |
| C. | 用甘氨酸和丙氨酸缩合最多可形成4种二肽 | |
| D. | 淀粉和纤维素互为同分异构 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
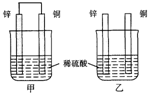
| A. | 两烧杯中铜片表面均无气泡产生 | |
| B. | 甲中铜片是正极,乙中铜片是负极 | |
| C. | 两烧杯中溶液的酸性均减弱 | |
| D. | 甲装置的导线中有电流,电流方向为锌→铜 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | B | C | D | |
| 电 极 | Zn C | Cu Ag | Zn Cu | Fe Zn |
| 溶 液 | 硫酸 | 硝酸银 | 蔗糖 | 硫酸 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
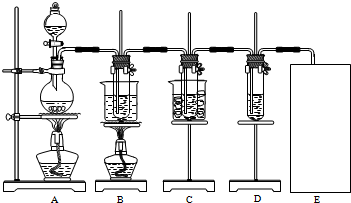
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
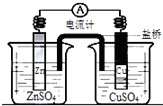
| A. | 铜是阳极,铜片上有气泡产生 | |
| B. | 锌离子在锌片表面被还原 | |
| C. | 正极附近的SO${\;}_{4}^{2-}$离子浓度逐渐增大 | |
| D. | 盐桥中的阳离子会移向CuSO4溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
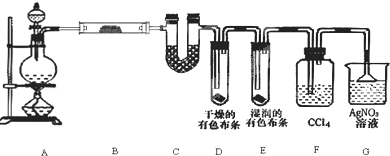
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铅蓄电池在放电过程中,负极质量减小,正极质量增加 | |
| B. | 一个化学反应是吸热还是放热,取决于反应物和生成物总能量的相对大小 | |
| C. | 一定条件下,使用催化剂能加快反应速率并提高反应物的平衡转化率 | |
| D. | 在原电池的负极和电解池的阴极上都发生失电子的氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com