

分析 维生素是参与生物生长发育和新陈代谢所必需的一类小分子有机化合物,种类较多包括维生素A、B、C、D、E等;钙、碘、氟、铁等元素是人体转化必需的元素,结合它们在人体中的作用分析;
解答 解:维生素A,别称抗干眼病维生素多存在于鱼肝油、动物肝脏、绿色蔬菜,缺少维生素A易患夜盲症;
维生素C亦称为抗坏血酸,多存在于新鲜蔬菜、水果;
钙元素是人体骨骼中的重要组成元素,缺钙易患佝偻病与骨质疏松;
碘元素有‘智力元素’之称,在人体中主要集中在甲状腺中,缺碘元素,易患甲状腺肿大;
氟元素是牙齿中的重要元素,缺少氟元素易患龋齿病;
铁元素在血液中是构成血红蛋白的元素,缺铁易患贫血病;
故答案为: .
.
点评 本题考查了常见营养物质在人体中的作用,题目难度不大,注意对基础知识的积累,明确维生素的分类和作用、以及Ca、Fe、I、F等元素在人体中的作用是解题的关键.


科目:高中化学 来源: 题型:选择题
| A. | 电池工作时锌为负极 | |
| B. | 电池正极的电极反应式为:2MnO2+2H2O+2e-═2MnOOH+2OH- | |
| C. | 电池工作时,电解液的OH-移向正极 | |
| D. | 外电路中每通过0.2mol电子,锌的质量理论上减少6.5g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
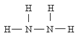 )可作为火箭发动机的燃料,NH3与NaClO反应可得到肼.
)可作为火箭发动机的燃料,NH3与NaClO反应可得到肼.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ③ | C. | ① | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
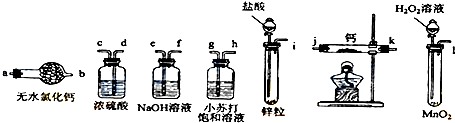
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com