
下列叙述正确的是()
A. 工业上电解熔融的Al2O3冶炼铝用铁做阳极
B. 用惰性电极电解Na2SO4溶液,阴、阳两极产物的物质的量之比为1:2
C. 用惰性电极电解饱和NaCl溶液,若有1mol电子转移,则生成1mol NaOH
D. 用惰性电极电解浓CuSO4溶液一小段时间后,加入Cu2O固体可以使CuSO4溶液恢复原来浓度
考点: 电解原理.
专题: 电化学专题.
分析: A、依据电解原理,铁做阳极,铁失电子生成亚铁离子,使阳极损耗;
B、电解硫酸钠溶液实质电解水,反应中阳极生成氧气,阴极生成氢气;
C、用惰性电极电解饱和NaCl溶液,生成氢氧化钠和氢气、氯气,2mol电子转移反应生成2mol氢氧化钠;
D、电解硫酸铜溶液生成氧气、硫酸和铜,加入CuO恢复溶液浓度,加入Cu2O固体发生氧化还原反应.
解答: 解:A、依据电解原理,铁做阳极,铁失电子生成亚铁离子,使阳极损耗,工业上是利用石墨做电解电解熔融的Al2O3冶炼铝,故A错误;
B、电解硫酸钠溶液实质电解水,反应中阳极生成氧气,阴极生成氢气,阴、阳两极产物的物质的量之比为2:1,故B错误;
C、用惰性电极电解饱和NaCl溶液,生成氢氧化钠和氢气、氯气,2mol电子转移反应生成2mol氢氧化钠,若有1mol电子转移,则生成1mol NaOH,故C正确;
D、电解硫酸铜溶液生成氧气、硫酸和铜,加入CuO恢复溶液浓度,加入Cu2O固体发生氧化还原反应不能恢复溶液浓度,故D错误;
故选C.
点评: 本题考查了电解原理的分析应用,主要是电解过程中产物的分析,氧化还原反应电子转移的计算应用,注意溶液浓度恢复的实质是出什么加什么,题目难度中等.


科目:高中化学 来源: 题型:
下列实验操作均要用玻璃棒,其中玻璃棒的作用及其目的相同的是()
①过滤 ②蒸发 ③溶解 ④向容量瓶转移液体.
A. ①和② B. ①和③ C. ③和④ D. ①和④
查看答案和解析>>
科目:高中化学 来源: 题型:
下列化学反应的离子方程式正确的是()
A. 氢氧化镁中滴加盐酸:H++OH﹣═H2O
B. 用FeCl3溶液腐蚀铜电路板:Fe3++Cu═Fe2++Cu2+
C. 在硫酸氢钾溶液中加入氢氧化钡溶液至pH=7:H++SO42﹣+Ba2++OH﹣═BaSO4↓+H2O
D. NH4HCO3溶液中加入过量NaOH溶液并加热:NH4++HCO3﹣+2OH﹣ NH3Ÿ+CO32﹣+2H2O
NH3Ÿ+CO32﹣+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
元素周期表是一座开放的“元素大厦”,40号元素在元素周期表中的位置是()
A. 第四周期第ⅡA族 B. 第五周期第ⅣB族
C. 第五周期第IVA族 D. 第五周期第ⅡA族
查看答案和解析>>
科目:高中化学 来源: 题型:
铅蓄电池是广泛应用于汽车、柴油机车等的启动电源.下列有关铅蓄电池的说法不正确的是()
A. 铅蓄电池在充电时,原来负极发生的反应是:Pb+SO42﹣﹣2e﹣⇌PbSO4
B. 铅蓄电池的电解质溶液是硫酸溶液,在放电过程中,它的浓度逐渐降低
C. 铅蓄电池在放电时,电子从Pb通过导线流向PbO2
D. 铅蓄电池放电时为原电池,充电时为电解池
查看答案和解析>>
科目:高中化学 来源: 题型:
铅蓄电池是工作时的电池反应为:PbO2+2H2SO4⇌2PbSO4+2H2O;试回答:
(3)铅蓄电池正极的电极材料是 .
(4)工作时该铅蓄电池负极的电极反应是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
将KO2放人密闭的真空容器中,一定条件下,发生反应:4KO2(s)⇌2K2O(s)+3O2(g),达到平衡后,保持温度不变,缩小容器体积,重新达到平衡.下列说法正确的是()
A. 容器内压强增大 B. KO2的量保持不变
C. 平衡常数减小 D. 氧气浓度不变
查看答案和解析>>
科目:高中化学 来源: 题型:
反应A(g)+3B(g)=4C(g)+2D(g),在不同条件下反应,其平均反应速率如下,其中反应速率最快的是()
A. v(A)=0.4mol/(L•s) B. v(B)=0.8mol/(L•s)
C. v(C)=1.2mol/(L•s) D. v(D)=0.7mol/(L•s)
查看答案和解析>>
科目:高中化学 来源: 题型:
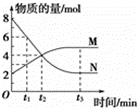
一定温度下,在2L的恒容密闭容器内发生的反应中M、N的物质的量随反应时间变化的曲线如图所示.
请回答下列问题:
(1)该反应的化学方程式为 .
(2)若t2=2min,N的平均反应速率为 .
(3)在t3时刻v正 (填“>”、“<”或“=”)v逆.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com