(2012?佛山二模)2012年2月27日深圳宣称进入“200万辆汽车时代”,汽车尾气已成为重要的空气污染物.
(1)汽车内燃机工作时引起反应:N
2(g)+O
2(g)?2NO(g),是导致汽车尾气中含有NO的原因之一.T℃时,向5L密闭容器中充入8mol N
2和9molO
2,5min后达平衡时NO物质的量为6mol,该反应的速率υ(NO)为
0.24mol?L-1?min-1
0.24mol?L-1?min-1
;计算该条件下的平衡常数
1.2
1.2
.
(2)恒温恒容,能说明反应 2NO(g)?N
2(g)+O
2(g) 达到平衡的是
AC
AC
(填代号).
A.单位时间内消耗2mol NO,同时消耗1mol N
2 B.NO、N
2、O
2的浓度之比为2:1:1
C.N
2的浓度不再发生变化
D.容器内气体密度不再发生变化
(3)H
2或CO可以催化还原NO以达到消除污染的目的:
①已知:N
2(g)+O
2(g)=2NO(g)△H=+180.5kJ/mol
2H
2(g)+O
2(g)=2H
2O(l)△H=-571.6kJ/mol
则H
2(g)与NO(g)反应生成N
2(g)和H
2O(l)的热化学方程式为:
2H2(g)+2NO(g)=N2(g)+2H2O(l)△H=-752.1kJ?mol-1
2H2(g)+2NO(g)=N2(g)+2H2O(l)△H=-752.1kJ?mol-1
.
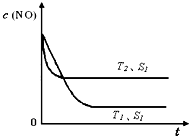
②当质量一定时,增大固体催化剂的表面积可提高化学反应速率.如图是反应:2NO(g)+2CO(g)?2CO
2(g)+N
2(g) 中NO的浓
度随温度(T)、催化剂表面积(S)和时间(t)的变化曲线,据此判断该反应的△H
<
<
0 (填“>”、“<”或“无法确定”).若催化剂的表面积S
1>S
2,在图中画出NO的浓度在T
1、S
2条件下达到平衡过程中的变化曲线,并注明条件.

 (2012?佛山二模)2012年2月27日深圳宣称进入“200万辆汽车时代”,汽车尾气已成为重要的空气污染物.
(2012?佛山二模)2012年2月27日深圳宣称进入“200万辆汽车时代”,汽车尾气已成为重要的空气污染物.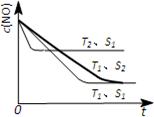 ,
, .
.

 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案