
计算题:
(Ⅰ).(6分)标准状况下,22.4LHCl气体溶于50ml水后再配成250m1溶液。
(1) 计算HCI的物质的量?
(2)计算所得盐酸的物质的量浓度?
(Ⅱ)(6分)某种待测浓度的H2SO4溶液5mL,加入10mL0.5mol/LBaCl2溶液,恰好完全反应。问得到BaSO4沉淀多少克?
(1)1m0L(3分)
(2)4m0l/L。(3分)
(Ⅱ)得到BaSO4沉淀1.165克。
【解析】
试题分析:标准状况下,22.4LHCl气体的物质的量: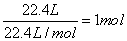
22.4LHCl气体溶于50ml水后再配成250m1溶液,所得盐酸的物质的量浓度: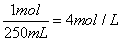
(Ⅱ)解:依题意,设得到BaSO4沉淀x,则
n(BaCl2) = 0.01L×0.5mol/L =" 0.005" mol 2分
H2SO4 + BaCl2 = BaSO4↓ + 2HCl 2分
1 mol 233g
0.005 mol x
∴ x =" 1.165" g 2分
答:得到BaSO4沉淀1.165克。
考点:物质的量、浓度及质量的计算
点评:考查物质的量计算及其相应的推导公式计算,计算简单,重在格式的书写及计算的精确考查。


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 压强/MPa 温度/℃ |
0.1 | 0.5 | 1 | 10 | 常压为1.01x105 =101kPa =0.1MPa |
| 400 | 99.2% | 99.6% | 99.7% | 99.9% | |
| 500 | 93.5% | 96.9% | 97.8% | 98.7% | |
| 600 | 73.7% | 85.8% | 89.5% | 96.4% |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com