
室温下,某溶液中水电离出的H+和OH-的物质的量浓度乘积为1×10-26,该溶液中一定不能大量存在的是( )
A.Cl-B.HCO3—C.Na+D.NO3—
 作业辅导系列答案
作业辅导系列答案 同步学典一课多练系列答案
同步学典一课多练系列答案 经典密卷系列答案
经典密卷系列答案 金牌课堂练系列答案
金牌课堂练系列答案科目:高中化学 来源:2014年高二化学人教版选修四 1化学反应与能量的变化练习卷(解析版) 题型:选择题
“摇摇冰”是一种即用即冷的饮料。吸食时,将饮料罐隔离层中的化学物质和水混合后摇动即会制冷。该化学物质是( )
A.氯化钠B.固体硝酸铵C.生石灰D.蔗糖
查看答案和解析>>
科目:高中化学 来源:2014年高二化学人教版选修四 15盐类水解的原理练习卷(解析版) 题型:填空题
(1)浓度均为0.01 mol·L-1的8种溶液:①HNO3 ②H2SO4 ③CH3COOH ④Ba(OH)2 ⑤NaOH
⑥CH3COONa ⑦KCl ⑧NH4Cl,这些溶液pH由小到大的顺序是(填写编号) 。
(2)pH=2的某酸HnA(An+为酸根)与pH=12的某碱B(OH)m混合,恰好反应生成正盐,混合液pH=8。
①反应生成的正盐的化学式为 。
②该盐中 离子一定能水解,其第一步水解的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源:2014年高二化学人教版选修四 14酸碱中和滴定练习卷(解析版) 题型:选择题
酸碱恰好完全中和时( )
A.酸与碱的物质的量一定相等
B.溶液呈现中性
C.酸与碱的物质的量浓度相等
D.酸所能提供的H+与碱所能提供的OH-的物质的量相等
查看答案和解析>>
科目:高中化学 来源:2014年高二化学人教版选修四 13pH的计算练习卷(解析版) 题型:选择题
常温下,柠檬酸水溶液的pH是3,食用醋的pH是2,可乐的pH是6,三种物质的溶液中c(OH-)分别是( )
A.1×10-11 mol·L-1,1×10-12 mol·L-1,1×10-8 mol·L-1
B.1×10-11 mol·L-1,1×10-8 mol·L-1,1×10-12 mol·L-1
C.2×10-11 mol·L-1,1×10-10 mol·L-1,1×10-8 mol·L-1
D.1×10-8 mol·L-1,1×10-11 mol·L-1,1×10-12 mol·L-1
查看答案和解析>>
科目:高中化学 来源:2014年高二化学人教版选修四 12水的电离 溶液的酸碱性练习卷(解析版) 题型:选择题
能影响水的电离平衡,并使溶液中的c(H+)>c(OH-)的操作是( )
A.向水中投入一小块金属钠B.将水加热煮沸
C.向水中通入CO2气体D.向水中加食盐晶体
查看答案和解析>>
科目:高中化学 来源:2014年高二化学人教版选修四 11弱电解质的电离练习卷(解析版) 题型:选择题
一元弱酸HA(aq)中存在下列电离平衡:HA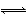 A-+H+。将1.0 mol HA分子加入水中制得1.0 L溶液,下图中,表示溶液中HA、H+、A-的物质的量浓度随时间而变化的曲线正确的是( )
A-+H+。将1.0 mol HA分子加入水中制得1.0 L溶液,下图中,表示溶液中HA、H+、A-的物质的量浓度随时间而变化的曲线正确的是( )
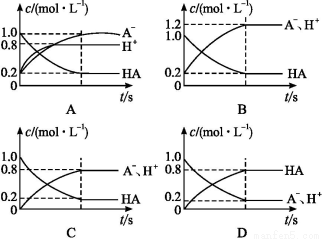
查看答案和解析>>
科目:高中化学 来源:2014年高二化学人教版选修二 模块综合检测练习卷(解析版) 题型:填空题
海南省是海洋大省,海水是一种丰富的资源,工业上从海水中可提取许多种物质,广泛应用于生活、生产、科技等方面。下图是某工厂对海水资源进行综合利用的示意图。
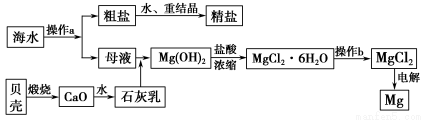
回答下列问题:
(1)流程图中操作a的名称为_________________________________________。
(2)工业上从海水中提取的NaCl,可用来制取纯碱,其简要过程如下:向饱和食盐水中先通入气体A,后通入气体B,充分反应后过滤得到晶体C和滤液D,将晶体C灼烧即可制得纯碱。
①则气体A应是_______________(填化学式),其过程反应方程式为_______________________________。
②滤液D中主要含有NH4Cl、NaHCO3等物质,工业上是向滤液D中通入NH3,并加入细小食盐颗粒,冷却析出不含有NaHCO3的副产品NH4Cl晶体,则通入NH3的作用是_______________________________________________。
(3)镁是一种用途很广的金属材料,目前世界上60%的镁从海水中提取。操作b是在__________气氛中进行,若在空气中加热,则会水解生成Mg(OH)Cl,写出有关反应的化学方程式_________________________________________。
(4)一氯碱厂每天消耗234吨NaCl,这些NaCl能生产质量分数为32%的烧碱溶液__________吨,同时转移__________mol电子。
查看答案和解析>>
科目:高中化学 来源:2014年高二化学人教版选修二 3单元综合检测练习卷(解析版) 题型:填空题
Ⅰ.工业上用铝土矿制取铝的流程如下:

请回答下列问题:
(1)操作Ⅰ、操作Ⅱ、操作Ⅲ都用到的玻璃仪器有__________________________。
(2)写出由溶液B生成Al(OH)3的离子方程式:____________________________。
(3)工艺流程中涉及氧化还原反应的化学方程式为:_________________________。
(4)生产过程中,除NaOH、H2O可以循环使用外,还可以循环使用的物质有________(填化学式)。用此法制取铝的副产品是________(填化学式)。
Ⅱ.我国高炉生产各方面取得了显著进步,但在资源和能源利用率、高炉大型化、提高产业集中度以及环保等方面还跟国际存在很大差距,有待进一步提高,努力向钢铁强国迈进。请回答下列问题:
(1)高炉炼铁的原料有铁矿、焦炭和石灰石,其中起熔剂作用的是________,目的是除去铁矿石中的脉石,其产物密度比铁________,所以在铁水的________(填“上部”或“下部”)形成炉渣而与铁水分离。
(2)焦炭在高炉炼铁中起着举足轻重的作用,下列不属于焦炭作用的是________。
A.作为燃料,为炼铁中的化学反应提供能量
B.作为还原剂与二氧化碳反应产生还原氧化铁的一氧化碳
C.对高炉中的物料起到支撑和疏散的作用
D.作为溶剂,除去铁矿石中的杂质
(3)高炉炼铁的污染非常严重,目前我国部分大城市中的钢铁厂借着搬迁的机会也在进行着工艺改进。高炉炼铁导致的环境污染有________。
A.臭氧空洞 B.酸雨 C.一氧化碳毒害 D.沙尘暴
(4)写出高炉炼铁中与碳元素有关的氧化还原反应化学方程式:____________________________。
(5)从“三废”利用、环境保护等角度考虑,钢铁企业在生产中应采取的一些措施有(举出2种措施即可) _______________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com