
【题目】下图是部分短周期元素原子(用字母表示)最外层电子数与原子序数的关系图。说法正确的是
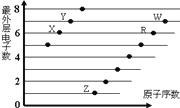
A. 元素的非金属性: X>R>W
B. 简单离子的半径:W>R>X
C. X与W形成的化合物中只有共价键
D. X与Z形成的化合物中只有离子键
【答案】C
【解析】由各原子的最外层电子数和原子序数的关系可推断X、Y、Z、R、W依次为O、F、Na、S、Cl元素。A项,元素的非金属性X(O)![]() R(S)、W(Cl)
R(S)、W(Cl)![]() R(S),错误;B项,根据“层多径大,序大径小”的原则,简单离子半径R(S2-)
R(S),错误;B项,根据“层多径大,序大径小”的原则,简单离子半径R(S2-)![]() W(Cl-)
W(Cl-)![]() X(O2-),错误;C项,O与Cl形成的化合物中只有共价键,正确;D项,X与Z可形成Na2O、Na2O2,Na2O中只有离子键,Na2O2中既有离子键又有共价键,错误;答案选C。
X(O2-),错误;C项,O与Cl形成的化合物中只有共价键,正确;D项,X与Z可形成Na2O、Na2O2,Na2O中只有离子键,Na2O2中既有离子键又有共价键,错误;答案选C。
同一主族元素 | 原子或离子半径从上而下依次增大 |
同一周期主族元素 | 原子半径从左到右逐渐变小 |
同种元素 | 原子半径大于阳离子半径;原子半径小于阴离子半径 |
电子层结构相同的离子 | 核电荷数越大,离子半径越小(阴前阳下,序大径小) |


科目:高中化学 来源: 题型:
【题目】化学与生产、生活、社会密切相关,下列说法不正确的是
A. 电动汽车充电、放电过程均有电子转移
B. 很多鲜花和水果的香味来自于酯
C. 淘米水能产生丁达尔效应,这种淘米水具有胶体的性质
D. 碳纳米管是一种比表面积大的有机合成纤维,可用作新型储氢材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着科学技术的不断进步,研究物质的手段和途径越来越多,H3、O4、C60、N5+等已被发现。下列有关说法中,正确的是( )
A. H2与H3属于同素异形体
B. O2与O4属于同位素
C. C60的质量数为 720 g/mol
D. N5+中含有36个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】加热N2O5依次发生的分解反应为:
①N2O5(g) ![]() N2O3(g)+O2(g)
N2O3(g)+O2(g)
②N2O3(g) ![]() N2O(g)+O2(g)
N2O(g)+O2(g)
在容积为2 L的密闭容器中充入8 mol N2O5,加热到t ℃,达到平衡状态后O2为9 mol,N2O3为3.4 mol。则平衡体系中N2O5的物质的量浓度为
A. 1.8mol/L B. 0.9 mol/L C. 2.3 mol/L D. 4.0 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于平衡体系:aA(g)+bB(g)![]() cC(g)+dD(g);正反应放热,有下列判断,其中正确的是
cC(g)+dD(g);正反应放热,有下列判断,其中正确的是
A. 若温度不变,容器体积扩大一倍,此时A的浓度是原来的0.45倍,则a+b>c+d
B. 若从正反应开始,平衡时A、B的转化率相等,则投入A、B物质的量之比为 a:b
C. 若平衡体系中共有气体M mol,再向其中充入bmolB,达到平衡时气体总物质的量为(M+b)mol,则a+b>c+d
D. 若a+b=c+d,则当容器内温度上升时,平衡向左移动,容器中气体的压强不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在 298 K、100 kPa 时,已知:2H2O(g)=O2(g)+2H2(g) ΔH1
Cl2(g)+H2(g)=2HCl(g) ΔH2
2Cl2(g)+2H2O(g)=4HCl(g)+O2(g) ΔH3
则 ΔH1 与 ΔH2 和 ΔH3 间的关系正确的是
A. ΔH3=ΔH1+2ΔH2 B. ΔH3=ΔH1+ΔH2
C. ΔH3=ΔH1-2ΔH2 D. ΔH3=ΔH1-ΔH2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与社会、科学、技术、环境、生活等有密切关系,下列说法正确的是
A. 燃煤中加入CaO可以减少酸雨的形成及温室气体的排放
B. 合成洗涤剂和纯碱溶液都可洗去油污的原理相同
C. 纤维素食用后在人体内水解为葡萄糖为人体提供能量
D. SO2具有还原性,可用已知浓度的KMnO4溶液测定食品中SO2残留量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知热化学方程式:
H2O(g)=H2(g) + 1/2O2(g) ΔH = +241.8kJ/mol
H2(g)+ 1/2O2(g) = H2O(1) ΔH = -285.8kJ/mol
当 1g 液态水变为水蒸气时,其热量变化是
A. 吸热 88kJ B. 吸热 2.44KJ C. 放热 44kJ D. 吸热 44KJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于金属及其化合物说法不正确的是( )
A.氧化铝用作耐火材料
B.小苏打用于食品膨松剂
C.目前用量最大的合金是铝合金
D.过氧化钠可作供氧剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com