
 ,它的名称是( )
,它的名称是( )| A. | 3-乙基丁烷 | B. | 3-乙基戊烷 | C. | 2-乙基丁烷 | D. | 3-甲基戊烷 |
分析 烷烃命名原则:
①长-----选最长碳链为主链;
②多-----遇等长碳链时,支链最多为主链;
③近-----离支链最近一端编号;
④小-----支链编号之和最小.看下面结构简式,从右端或左端看,均符合“近-----离支链最近一端编号”的原则;
⑤简-----两取代基距离主链两端等距离时,从简单取代基开始编号.如取代基不同,就把简单的写在前面,复杂的写在后面.
解答 解:该有机物主链有5个C,3号位有1个甲基,则 的名称是3-甲基戊烷,故选D.
的名称是3-甲基戊烷,故选D.
点评 本题考查了有机物的命名,题目难度中等,该题注重了基础性试题的考查,侧重对学生基础知识的检验和训练,该题的关键是明确有机物的命名原则,然后结合有机物的结构简式灵活运用即可,有利于培养学生的规范答题能力.


 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:解答题
 液480mL.
液480mL.查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 若将乙池电解液换成AgNO3溶液,则可以实现在石墨棒上镀银 | |
| B. | 甲池通入CH3OH的电极反应式为CH3OH+6e-+2H2O═CO$\stackrel{2-}{3}$+8H+ | |
| C. | 反应一段时间后,向乙池中加入一定量Cu(OH)2固体,能使CuSO4溶液恢复到原浓度 | |
| D. | 甲池中消耗224mL(标准状况下)O2,此时丙池中理论上产生1.16g固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l) | B. | (NH4)2CO3(s)═NH4HCO3(g)+NH3(g) | ||
| C. | 2CO(g)+O2(g)$\frac{\underline{\;点燃\;}}{\;}$2CO2(g) | D. | 2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$Al2O3+2Fe |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
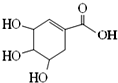
| A. | 分子式为C7H10O5 | |
| B. | 分子中含有3种官能团 | |
| C. | 可发生加成和取代反应 | |
| D. | 在水溶液中羟基和羧基均能电离出氢离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH3的摩尔质量为17g | |
| B. | 48gO3含有的臭氧分子数为6.02×1023 | |
| C. | 1mol•L-1NaCl溶液中含1molNa+ | |
| D. | 标准状况下,1molH2O的体积为22.4 L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 碳酸氢铵是一种重要的铵盐.实验室中,将二氧化碳通入氨水可制得碳酸氢铵.在精制饱和食盐水中加入碳酸氢铵可制备小苏打(NaHCO3),并提取氯化铵作为肥料或进一步提纯为工业氯化铵.完成下列填空:
碳酸氢铵是一种重要的铵盐.实验室中,将二氧化碳通入氨水可制得碳酸氢铵.在精制饱和食盐水中加入碳酸氢铵可制备小苏打(NaHCO3),并提取氯化铵作为肥料或进一步提纯为工业氯化铵.完成下列填空:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com