
| A. | 信息产业中的光缆的主要成份是单质硅 | |
| B. | NO2、CO2、SO2、PM2.5颗粒都会导致酸雨 | |
| C. | 高铁车厢大部分材料采用铝合金,因铝合金强度大、质量轻、抗腐蚀能力强 | |
| D. | 发酵粉能使焙制出的糕点疏松多孔,是因为发酵粉中含有碳酸氢钠 |
分析 A.光导纤维是信息技术的基石,主要成分是SiO2,硅常用作太阳能电池的原料;
B.PM2.5是造成灰霾天气的“元凶”之一,与酸雨无关,二氧化碳不是形成酸雨的物质;
C.车厢大部分采用铝合金材料制造,这是因为铝合金具有质量轻,强度大,抗腐蚀能力比较强的优点;
D.碳酸氢钠受热分解出二氧化碳,使焙制出的糕点疏松多孔.
解答 解:A.光导纤维的主要成分是二氧化硅,有良好的导光性,硅常用作太阳能电池的原料,故A错误;
B.酸雨是指溶液pH小于5.6的雨水,正常雨水的pH约为5.6,二氧化硫、氮氧化物等物质是形成酸雨的重要物质,二氧化碳排放过多会引起温室效应,不是形成酸雨的气体,PM2.5是造成灰霾天气的“元凶”之一,所以CO2、PM2.5颗粒都不会导致酸雨,故B错误;
C.铝常温下能与空气中氧气反应,生成一层致密的氧化物保护膜,从而具有抗腐蚀性,铝合金材料的密度小,用以减轻列车质量,铝合金强度大,所以高铁车厢大部分材料采用铝合金,故C正确;
D.发酵粉中含有碳酸氢钠,碳酸氢钠受热分解出二氧化碳,使焙制出的糕点疏松多孔,故D正确;
故选CD.
点评 本题主要考查了材料的使用、环境保护等知识,掌握光纤的成分、酸雨、合金的用途、发酵粉等基础知识是解答本题的关键,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | X的金属性比Y的金属性强 | |
| B. | 常温下,X和Y都不能从水中置换出氢 | |
| C. | Y元素的氢氧化物碱性比X元素的氢氧化物碱性大 | |
| D. | X元素的最高化合价比Y元素的最高化合价低 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
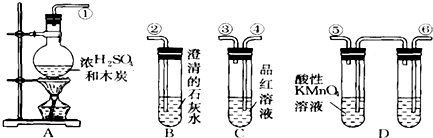
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
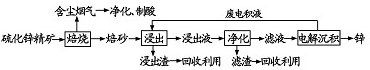
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 所用氢氧化钠已经潮解 | |
| B. | 向容量瓶中加水未到刻度线 | |
| C. | 有少量氢氧化钠溶液残留在烧杯里 | |
| D. | 用带游码的托盘天平称2.4 gNaOH时误用了“左码右物”方法 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
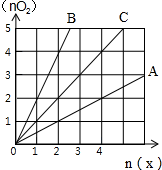
| A. | 2:1 | B. | 1:2 | C. | 1:1 | D. | 任意 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | A | |||||||
| 2 | B | C | D | E | ||||
| 3 | F | G | H | I | J | K | M | N |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化硫可用于纸浆漂白,表明二氧化硫具有还原性 | |
| B. | 煤经过气化和液化等物理变化可以转化为清洁燃料 | |
| C. | 为防止月饼等富脂食品氧化变质,常在包装袋中放入生石灰 | |
| D. | Na2O2可用作呼吸面具的供氧剂 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com