
【题目】W、X、Y、Z四种短周期元素的原子序数X>W>Z>Y.W原子的最外层没有p电子,X原子核外s电子与p电子数之比为1:1,Y原子最外层s电子与p电子数之比为1:1,Z原子核外电子中p电子数比Y原子多2个.
(1)X元素的单质与Z、Y所形成的化合物反应,其化学方程式:__________________.
(2)W、X元素的最高价氧化物对应水化物的碱性强弱为__________(用分子式表示).
(3)四种元素原子半径的由大到小为_________(填元素符号).
【答案】2Mg+CO2![]() 2MgO+CMg(OH)2<NaOHNa>Mg>C>O
2MgO+CMg(OH)2<NaOHNa>Mg>C>O
【解析】
短周期元素中,Y原子最外层s电子与p电子数之比为1:1,最外层电子排布为ns2np2,处于ⅣA族,X原子核外s电子与p电子数之比为1:1,原子核外电子排布为1s22s22p4或1s22s22p63s2,W、X、Y、Z四种短周期元素的原子序数X>W>Z>Y,X、Y应分别为1s22s22p63s2 、1s22s22p2,即X为镁,Y为碳,Z原子核外电子中p电子数比Y 原子多2个,Z为O元素,W原子的最外层没有p电子,则W为钠。
(1) X元素的单质为镁,与Z、Y所形成的化合物反应,即化合物为二氧化碳,二者反应生成氧化镁和碳,方程式为:2Mg+CO2![]() 2MgO+C; (2) 同一周期自左到右金属性减弱,元素的最高价氧化物对应水化物的碱性减弱,所以碱性关系为Mg(OH)2<NaOH ; (3)同周期元素从左到右原子半径逐渐较小,同主族元素从上到下原子半径逐渐增大,故原子半径关系为Na>Mg>C>O。
2MgO+C; (2) 同一周期自左到右金属性减弱,元素的最高价氧化物对应水化物的碱性减弱,所以碱性关系为Mg(OH)2<NaOH ; (3)同周期元素从左到右原子半径逐渐较小,同主族元素从上到下原子半径逐渐增大,故原子半径关系为Na>Mg>C>O。


科目:高中化学 来源: 题型:
【题目】在20℃,5.05×105Pa条件下,密闭容器中进行反应2A(g)+xB(g)![]() 4C(g),达平衡时c(A)=1.00molL-1,现将压强减小到1.01×105Pa,建立平衡后,c(A)=0.18molL-1,则下列说法正确的是 ( )
4C(g),达平衡时c(A)=1.00molL-1,现将压强减小到1.01×105Pa,建立平衡后,c(A)=0.18molL-1,则下列说法正确的是 ( )
A.系数x >2
B.若增大该体系的压强,平衡向左移动,化学平衡常数变小
C.若增大该体系的压强,平衡向右移动,化学平衡常数不变
D.该反应的化学平衡常数表达式是K=![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关蛋白质的叙述中不正确的是( )
A.向蛋白质溶液滴加硫酸铜溶液发生盐析
B.蛋白质遇浓硝酸显黄色
C.蛋白质溶液具有丁达尔效应
D.蛋白质的基本结构单元是氨基酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组中的两种物质作用时,反应条件(温度、反应物用量、浓度等)改变,不会引起产物改变的是 ( )
A. NaOH和CO2B. Fe粉在Cl2中燃烧
C. Na和O2D. Cu和HNO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,将0.10 mol·L-1盐酸逐滴滴入20.00 mL 0.10 mol·L-1氨水中,溶液中pH和pOH随加入盐酸体积变化曲线如图所示。已知:pOH= -lg c(OH-)。下列说法正确的是( )
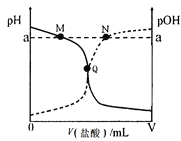
A. M点所示溶液中:c(NH4+)+c(NH3·H2O)= c(Cl-)
B. N点所示溶液中:c(NH4+)>c(Cl-)
C. Q点所示消耗盐酸的体积等于氨水的体积
D. M点和N点所示溶液中水的离子积相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中,正确的是 ( )
A. H2SO4的摩尔质量是98
B. 等质量的CO与CO2中所含碳原子数之比为7︰11
C. 等质量的O2和O3中所含的氧原子数相同
D. 98g H2SO4溶解于500mL 所得溶液中硫酸的物质的量浓度为2 molL-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同学们在实验室里用不同的方法分别制取Cu(NO3)2,并在此基础上探究Cu(NO3)2的化学性质。
(1)甲组同学直接用铜屑与稀硝酸反应制取Cu(NO3)2,反应的化学方程式是___。
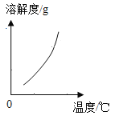
(2)乙组同学查阅了硝酸铜晶体的溶解度曲线(下图),据此设计了以下实验方案,先将铜粉在空气中充分灼烧,再将灼烧后的物质与适量稀HNO3反应,欲从反应后的溶液中得到Cu(NO3)2晶体,依次进行的操作是:蒸发浓缩、____________、过滤、洗涤、干燥。乙组同学认为此方案优于甲组的方案,理由之一是_____。
(3)丙组同学用Cu(NO3)2晶体,探究其热稳定性,实验装置如下所示。(夹持装置和加热仪器未画出)

①充分加热Cu(NO3)2晶体一段时间后,观察到U形管中气体变为红棕色,红棕色气体是____________。
②集气瓶中最终收集到的气体颜色是____________,U形管中进入集气瓶后颜色发生变化的原因是___。
③欲证明试管中残留的黑色粉末是CuO[假设Cu(NO3)2晶体已全部分解],实验方案是___。
④由该实验可得出的结论是___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com