
����Ŀ����������(H)������ʳ���㾫���÷�����AΪԭ���Ⱥϳ������G(![]() )���̶��ϳ�H��·�����£�
)���̶��ϳ�H��·�����£�
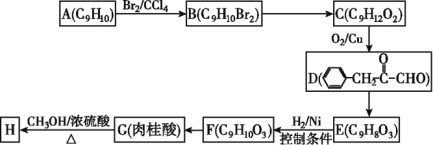
��ش���������:
(1)������A�Ľṹ��ʽΪ_____________��D�к��й����ŵ�����Ϊ_________________��
(2)B��C�����Լ���������______________��F��G�ķ�Ӧ����Ϊ__________��
(3)G��H�Ļ�ѧ����ʽΪ______________________________��
(4)д��������ụΪͬ���칹�壬����ʹ������Ȼ�̼��Һ��ɫ,������̼��������Һ��Ӧ������ͬ���칹��Ľṹ��ʽ_______________________________��
���𰸡�![]() �ʻ���ȩ�� NaOHˮ��Һ ��ȥ��Ӧ
�ʻ���ȩ�� NaOHˮ��Һ ��ȥ��Ӧ ![]() +CH3OH
+CH3OH ![]()
![]() +H2O
+H2O ![]() ��
��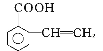 ��
��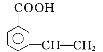 ��
��
��������
C�IJ����Ͷ�=![]() =4��C�IJ����Ͷ�Ϊ4�����D�ṹ��ʽ֪��C�к���һ��������C�ṹ��ʽΪ
=4��C�IJ����Ͷ�Ϊ4�����D�ṹ��ʽ֪��C�к���һ��������C�ṹ��ʽΪ![]() ��B����ȡ����Ӧ��ˮ�ⷴӦ����C��B�ṹ��ʽΪ
��B����ȡ����Ӧ��ˮ�ⷴӦ����C��B�ṹ��ʽΪ![]() ��A�����ӳɷ�Ӧ����B��A�ṹ��ʽΪ
��A�����ӳɷ�Ӧ����B��A�ṹ��ʽΪ![]() �����E����ʽ֪��D����������Ӧ����E��E�ṹ��ʽΪ
�����E����ʽ֪��D����������Ӧ����E��E�ṹ��ʽΪ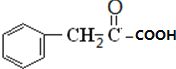 ��E�����ӳɷ�Ӧ���F����ʽ֪��F�ṹ��ʽΪ
��E�����ӳɷ�Ӧ���F����ʽ֪��F�ṹ��ʽΪ![]() ��F������ȥ��Ӧ����G��
��F������ȥ��Ӧ����G��![]() ��G��״�CH3OH����������Ӧ����H��H�ṹ��ʽΪ
��G��״�CH3OH����������Ӧ����H��H�ṹ��ʽΪ![]() ���ݴ˷������
���ݴ˷������
(1)ͨ�����Ϸ���֪��A�Ľṹ��ʽΪ![]() ��D�й��������ʻ���ȩ����
��D�й��������ʻ���ȩ����
(2)B��![]() ��B��±��������NaOHˮ��Һ�з���ȡ����Ӧ����C
��B��±��������NaOHˮ��Һ�з���ȡ����Ӧ����C![]() ��F��
��F��![]() ����Ũ�����ڼ��������·�����ȥ��Ӧ����G��
����Ũ�����ڼ��������·�����ȥ��Ӧ����G��![]() ������F��G�ķ�Ӧ��������ȥ��Ӧ��
������F��G�ķ�Ӧ��������ȥ��Ӧ��
(3)G��![]() ����״�CH3OH��Ũ�������ʱ���ڼ��������·���������Ӧ����H��
����״�CH3OH��Ũ�������ʱ���ڼ��������·���������Ӧ����H�����÷�Ӧ�Ļ�ѧ����ʽΪ
![]() +CH3OH
+CH3OH![]()
![]() +H2O��
+H2O��
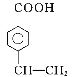
(4)������ụΪͬ���칹�壬����ʹ������Ȼ�̼��Һ��ɫ��˵���������ں��в�����̼̼����������̼��������Һ��Ӧ��˵�������Ȼ�������������ͬ���칹��ṹ��ʽΪ
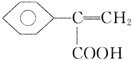 ��
�� ��
��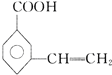 ��
��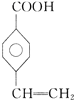 ��
��


 ȫ�ܲ����ĩС״Ԫϵ�д�
ȫ�ܲ����ĩС״Ԫϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������0.1 mol/L AgNO3��Һ��0.1 mol/L NaCl��Һ��ϵõ���Һ�����˺��������ʵ�飺
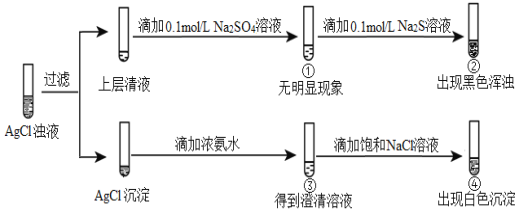
���з�������ȷ����
A. �ٵ�����˵���ϲ���Һ�в���Ag+
B. �ڵ�����˵�����¶���Ag2S��Ag2SO4������
C. ��������Ag(NH3)2+���ٽ�AgCl(s)�ܽ�ƽ�������ƶ�
D. ������еμ�һ���������ᣬҲ���Գ��ְ�ɫ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��صĹ���ԭ����ͼ��ʾ�������Ϊ���軯��K3[Fe(CN)6]�������軯��K4[Fe(CN)6]�Ļ����Һ������˵������ȷ���ǣ� ��
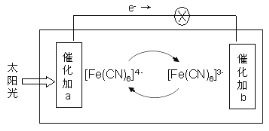
A��K+�������b
B������a���淢���Ļ�ѧ��Ӧ��[Fe(CN)6]4- - e- = [Fe(CN)6]3-
C��[Fe(CN)6]3-�ڴ���b���汻����
D���������Һ�е�[Fe(CN6)]4-��[Fe(CN6)]3-Ũ�Ȼ������ֲ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1��ͼΪ����ȼ�ϵ��ԭ��ʾ��ͼ�����մ�ͼ����ʾ���ش��������⣺
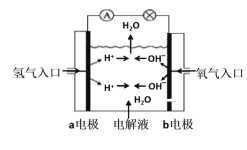
��������������ȷ����___��
A.a�缫�Ǹ���
B.b�缫�ĵ缫��ӦΪ��4OH--4e-=2H2O+O2��
C.����ȼ�ϵ����һ�־���Ӧ��ǰ������ɫ��Դ
D.����ȼ�ϵ����һ�ֲ���Ҫ����ԭ����������ȫ�������ڵ���ڵ����ͷ���װ��
�����������ҺΪKOH��Һ����缫��ӦʽΪ��a��__��b��___��
��2�������⻯����NaBH4(BԪ�صĻ��ϼ�Ϊ+3��)��H2O2��ԭ�ϵ�ȼ�ϵ�أ��������ϲ���Pt/C���������ϲ���MnO2���������վ�ͨ�����ǵ�Դ���乤��ԭ����ͼ��ʾ���ش��������⣺
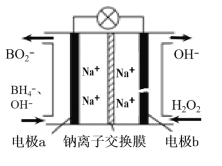
�ٵ�طŵ�ʱNa+�ƶ������ǣ�__����������������������������������
�ڵ缫b����MnO2��MnO2��������__��
�۸õ�صĸ�����ӦΪ��__��
��ÿ����3molH2O2��ת�Ƶĵ�����Ϊ__��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2014��5��7�գ����ij���̼�˾�ڽ���̽����ҵ�ڼ䣬һö�ƶ�����С�ķ���Դҿ-192��ʧ����������صİ�ȫ�¹ʣ�ͼʾ��ҿ��Ԫ�����ڱ��е���Ϣ������˵����ȷ���ǣ� ��
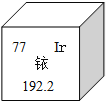
A. ҿ�����ԭ������Ϊ192.2��
B. ҿԭ�Ӻ��ڵ�������Ϊ77
C. K2IrO3��Ir�Ļ��ϼ�Ϊ+4
D. �����г��õ�ҿ���Ϊ������ҿ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�Dz��ֶ�����Ԫ��ԭ�Ӱ뾶��ԭ�������Ĺ�ϵͼ����X��Y��Z��M��N��PΪ���ţ���ΪԪ�ط��ţ�������˵����ȷ���ǣ� ��
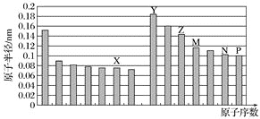
A.Z��N����Ԫ�ص����Ӱ뾶��ȣ�ǰ�߽ϴ�
B.N��P����Ԫ�ص���̬�⻯����ȶ�����ȣ�ǰ�߽��ȶ�
C.��X��M����Ԫ����ɵĻ����ﲻ�����κ��ᷴӦ��������ǿ�Ӧ
D.Z���������ֱܷ��ܽ���Y�����������P���⻯���ˮ��Һ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ģ�ҵ�����ӽ���Ĥ�����ռ�ķ���������������Һ���Ʊ�������������������������أ�װ����ͼ��ʾ������˵������ȷ���ǣ�������
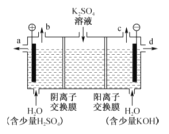
A. ͨ�翪ʼ������������ҺpH����
B. �Ƶõ�����������Һ�ӳ���d����
C. ���۵�������ӦʽΪ2H2O��4e-��4H++O2��
D. ͨ�������ӽ���Ĥ������������ͨ�������ӽ���Ĥ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ɫ�����ĩ������Cu��Cu2O��Fe2O3�е�һ�ֻ��֡�Ϊ̽������ɣ���ȡa g�ù����ĩ��Ʒ���ù�����ϡ�����ַ�Ӧ��(��֪:Cu2O+2H+��Cu2++Cu+H2O)���Ƶù�������Ϊb g���������ƶϲ���������
A. ��Ӧ����Һ�д������ڵ������������3��
B. ��Ӧ�����Һ�м���һ������NaNO3������ʹb g������ȫ�ܽ�
C. ��b��![]() a�����ɫ�����ĩһ��Ϊ������
a�����ɫ�����ĩһ��Ϊ������
D. b��ȡֵ��Χ:0��b��a
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��CO2��һ�����۵�̼��Դ�����ۺ����þ�����Ҫ���塣�ش��������⣺
��1��CO2���Ա�NaOH��Һ������������ҺpH=13��CO2��Ҫת��Ϊ___________��д���ӷ��ţ�����������Һc(HCO3)��c(CO32)=2��1����ҺpH=___________���������£�H2CO3��K1=4��107��K2=5��1011��
��2��CO2��CH4�����������Ƶúϳ�����CH4(g)+ CO2(g) ![]() 2CO (g)+ 2H2(g)
2CO (g)+ 2H2(g)
��֪������Ӧ����صĻ�ѧ�������������£�
��ѧ�� | C��H | C=O | H��H | C |
����/kJ��mol1 | 413 | 745 | 436 | 1075 |
��÷�Ӧ����H=______���ֱ���VL�����ܱ�����A�����ݣ���B����ѹ���ݻ��ɱ䣩�У�����CH4��CO2��1 mol�Ļ�����塣�������з�Ӧ��ƽ���ų������յ������϶����____������A�� ����B ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com