
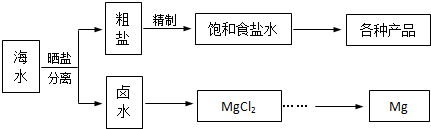
| 物质 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 | Mg(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 8.3 | 9.6 |
| 沉淀完成 | 3.7 | 9.6 | 9.5 | 11.1 |
| ||
| 0.01mol |
| 0.1L |
| 1×10-14 |
| 0.1 |
| ||
| ||


科目:高中化学 来源: 题型:
| A、加入氯化钡溶液有白色沉淀生成,再加稀硝酸,沉淀不消失,一定有硫酸根离子 |
| B、钾元素焰色反应的操作是:将铂丝放在稀盐酸中洗涤后灼烧至无色,然后再用铂丝蘸取固体氯化钾,进行灼烧,直接观察火焰颜色 |
| C、加入NaOH溶液,加热,放出能使湿润的红色石蕊试纸变蓝的气体,证明一定含有NH4+ |
| D、加入AgNO3溶液,有白色沉淀生成,证明含有Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
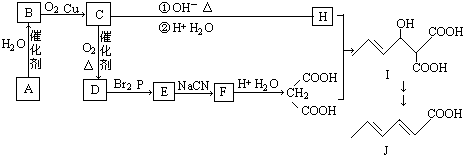
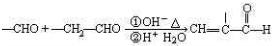
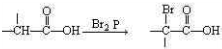
查看答案和解析>>
科目:高中化学 来源: 题型:
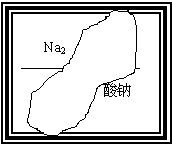 某同学在帮助老师整理实验室的化学试剂时,发现一盛有无色溶液的试剂瓶,由于腐蚀,其标签已破损(如图:标签上部的化学式和下部的名称都不完整),根据前几天做过的实验判断,它是中学化学中常见的溶液.
某同学在帮助老师整理实验室的化学试剂时,发现一盛有无色溶液的试剂瓶,由于腐蚀,其标签已破损(如图:标签上部的化学式和下部的名称都不完整),根据前几天做过的实验判断,它是中学化学中常见的溶液.| 推测(写化学式) | 依据的实验操作(加入验证试剂)、现象和结论 |
| 例:Na2SiO3 | 加入盐酸,若只有白色沉淀生成者为硅酸钠溶液 |
| ①: | |
| ②: | |
| ③: | |
| ④: |
查看答案和解析>>
科目:高中化学 来源: 题型:
| X | ||
| M |
查看答案和解析>>
科目:高中化学 来源: 题型:
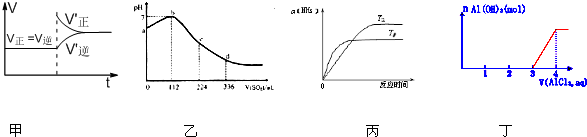
| A、甲图表示可逆反应:3Fe(s)+4H2O(g)?Fe3O4(s)+4H2 (g)增大压强后,V正、V逆变化图 |
| B、乙图是标准状况下,某同学向100mL H2S饱和溶液中通入SO2,所得溶液pH变化图.由图可知ab段反应是:SO2+2H2S═3S↓+2H2O |
| C、丙图表明合成氨反应温度与转化率之间的关系,由图知合成氨反应是吸热反应 |
| D、丁图表明向一定量的NaOH溶液中逐滴加入AlCl3溶液的反应.说明反应分两步:①Al3++3OH-=Al(OH)3↓②Al(OH)3+OH-=AlO2-+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、我国居民传统膳食以糖类为主,淀粉、脂肪都是糖类物质 |
| B、人体内的蛋白质不断分解,最终生成水和二氧化碳排出体外 |
| C、乙醇可以被氧化为乙酸,二者均能发生酯化反应 |
| D、用氢氧化钠溶液可除去乙酸乙酯中混有的少量的乙酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
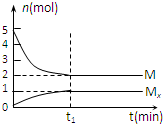 E是非金属性最强的元素,M是E的气态氢化物,在一定体积的密闭容器中,气体M存在如下关系:aM(g)?bMx(g ),反应物和生成物的物质的量随时间的变化关系如图.下列说法正确的是( )
E是非金属性最强的元素,M是E的气态氢化物,在一定体积的密闭容器中,气体M存在如下关系:aM(g)?bMx(g ),反应物和生成物的物质的量随时间的变化关系如图.下列说法正确的是( )| A、该反应的化学方程式是2HF?(HF)2 |
| B、时刻,保持温度不变,再充入5molM,重新达到平衡时,将减小 |
| C、平衡时混合气体的平均摩尔质量是33.3g/mol |
| D、M的沸点比同主族下一周期元素的气态氢化物沸点低 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com