



 科学实验活动册系列答案
科学实验活动册系列答案科目:高中化学 来源: 题型:
| A、遇苯酚显紫色的溶液:I-、AlO2-、SCN-、Mg2+ |
| B、pH=12的溶液:AlO2-、ClO-、SO32-、Na+ |
| C、含较多Al3+离子的溶液:Na+、NO3-、S2-、AlO2- |
| D、pH=2的HNO3溶液:Na+、Ag+、NO3-、NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
 某小组为研究电化学原理,设计如图装置.下列叙述不正确的是( )
某小组为研究电化学原理,设计如图装置.下列叙述不正确的是( )| A、a和b不连接时,铁片上会有金属铜析出 |
| B、a和b用导线连接时,铜片上发生的反应为:Cu2++2e-=Cu |
| C、无论a和b是否连接,铁片均会溶解,溶液从蓝色逐渐变成浅绿色 |
| D、a和b用导线连接时,可形成原电池,其中阳离子向负极移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.5mol/L氢氧化钙溶液和0.5mol/L碳酸氢镁溶液等体积混合反应:Ca2++OH-+HCO3-=CaCO3↓+H2O |
| B、少量的SO2通入Ca(ClO)2溶液中反应的离子方程式为:SO2+H2O+Ca2++2ClO-=CaSO3↓+2HClO |
| C、将11.2L标准状况下的氯气通入200mL 2mol/L的FeBr2溶液中,离子反应方程式为:2Fe2++8Br-+5Cl2═2Fe3++4Br2+10Cl- |
| D、某锂电池电极总反应为:4Li+2SOCl2=4LiCl+S+SO2↑,则正极反应为:2SOCl2+4e-=4Cl-+S+SO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、元素X、M组成的化合物中阴阳离子个数之比为1:2 |
| B、气态氢化物的稳定性:Z<W |
| C、X、Y和M三种元素形成的化合物的水溶液呈碱性 |
| D、W元素的含氧酸都属于强酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| T/℃ | 165 | 175 | 185 | 195 |
| K | 111.9 | 74.1 | 50.6 | 34.8 |
| n(NH3) |
| n(CO2) |
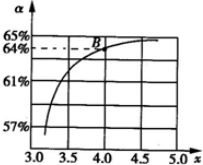

查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素A | s电子总数是p电子总数的2倍 |
| 元素C | 某种核素原子的质量数为18,中子数为10 |
| 元素X | 单质是良好的半导体材料 |
| 元素Y | 其单质为淡黄色晶体,常用来处理打碎的水银温度计 |
| 元素Z | 3d能级上有4个未成对电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温常压下,16g O3气体含有氧原子数为NA |
| B、标准状况下,44.8L四氯化碳含有的分子数为2NA |
| C、0.1mol?L-1氯化铝溶液中含有Al3+数为0.1NA |
| D、2.4g金属镁变为镁离子时失去的电子数为0.1NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com