
| A. | $\frac{n(m-x+2)}{m}$ mol | B. | $\frac{n(m-x)}{m}$ mol | C. | $\frac{m-x+2}{m-n}$ mol | D. | $\frac{n(m-x-2)}{m}$ mol |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | SO3+H2O═H2SO4 | B. | Cl2+H2O═HCl+HClO | ||
| C. | 2F2+2H2O═4HF+O2 | D. | 2Na+2H2O═2NaOH+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子化合物中一定含有金属元素 | |
| B. | 只由共价键构成的物质不一定是共价化合物 | |
| C. | 原煤、天然气属于一次能源,而电力、蒸汽则属于二次能源 | |
| D. | 锌锰电池是一次电池,而铅蓄电池则是二次电池 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
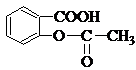 转变为
转变为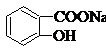 的方法是( )
的方法是( )| A. | ①② | B. | ①④ | C. | ②③ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| X | Y | Z | |
| W | |||
| T |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com