
����Ŀ���칬һ����2011��9��29��21ʱ16��3���ھ�Ȫ���Ƿ������ķ��䣬�칬һ�����ɳ������Ŵ���������������յģ�����ƽ����dzɹ�����������Ҫ���أ��ƽ����ķ�չ����һ�������Ĺ��̣�
��1��20����ǰ���ڻ�ҩ��������Ψһ�Ļ�����ƽ������ڻ�ҩ��������ء���ǡ�ľ̿��ɣ��ڻ�ҩ��ը�Ļ�ѧ����ʽ��2KNO3+S+3C�TK2S+N2��+3CO2����
��������Ӧ�е���������_____������0.5mol S�μӷ�Ӧ����ת�Ƶĵ��ӵ����ʵ���Ϊ_____mol��
��ij��ѧ��ȤС�����������ʵ�飺
ʵ��һ��ȡ�����ڻ�ҩ����ˮ�����ˣ�����Һ����Ũ������ȴ����������Ũ���ᣬ�����Һ�����Թ��в�����ͭƬ��������������ɫ���壬д���÷�Ӧ�����ӷ���ʽ_______��
ʵ�����ȡ�ڻ�ҩ��ը��IJ������壬��ˮ�ܽ���ˣ�ȡ��Һ�����еμ�������ˮ��������һ��ʼ��Һ����Ǻ��ֱ���壮����ǵ�������_____����ѧʽ��ʾ����
���ʵ�鷽��֤���ó���Һ�к���Cl��_____��
��2��1947�꣬���Ƴ��ڶ���������������李����۸����ƽ��������������ײ�����������ұ�ը���䱬ը������4�֣�2�ֲ����ǿ����е���Ҫ�ɷ֣���һ�����������ʹʪ�����ɫʯ����ֽ��죬д���÷�Ӧ�Ļ�ѧ����ʽ_____��
��3������ƽ���һ�㶼���е�Ԫ�أ���������������ḻ����ѧ�Ҵӻ��ʳ�������������м�����ΪN4H4��SO4��2�����ʣ�������Ϊ������ˮ��ǿ����ʣ����ռ������N4���壬�÷�Ӧ�����ӷ���ʽ_____��
���𰸡� KNO3��S 6 Cu+4H++2NO3-=Cu2++2NO2��+2H2O�� S ����Һ�м������������ữ����������Һ,����а�ɫ��������˵���������� ![]() N4H44++4OH-= N4��+4H2O
N4H44++4OH-= N4��+4H2O
��������(1)���÷�Ӧ��NԪ�ػ��ϼ���+5�۱�Ϊ0�ۡ�SԪ�ػ��ϼ���0�۱�Ϊ-2�ۡ�CԪ�ػ��ϼ���0�۱�Ϊ+4��,�õ��ӻ��ϼ۽��͵ķ�Ӧ�������������÷�Ӧ��ֻ��C�ǻ�ԭ�������ݷ���ʽ֪,�����0.5molS �μӷ�Ӧ,����1.5molC �μӷ�Ӧ,����C��ת�Ƶ���֮���ϵʽ����ת�Ƶ������ʵ�����
������������,��������Ӿ���ǿ������,������Cu����ͭ����,��������ԭ����NO2����������ǿ������,������������������S�������������������ữ����������Һ����,����Һ�м������������ữ����������Һ,����а�ɫ��������˵������������
(2)���������ײ�����������ұ�ը,�䱬ը������4��,2�ֲ����ǿ����е���Ҫ�ɷ�Ϊ����������,��һ�����������ʹʪ�����ɫʯ����ֽ���,Ϊ����,����ԭ���غ�֪������ˮ������
(3) N4H4��SO4��2Ϊ������ˮ��ǿ�����,���ռ������N4����,�����ӽ����������������N4�����ˮ��
(1)���÷�Ӧ��NԪ�ػ��ϼ���+5�۱�Ϊ0�ۡ�SԪ�ػ��ϼ���0�۱�Ϊ-2�ۡ�CԪ�ػ��ϼ���0�۱�Ϊ+4��,�õ��ӻ��ϼ۽��͵ķ�Ӧ����������,����KNO3��S �����������÷�Ӧ��ֻ��C�ǻ�ԭ��,���ݷ���ʽ֪,�����0.5molS �μӷ�Ӧ,����1.5molC�μӷ�Ӧ,����C��ת�Ƶ���֮���ϵʽ��ת�Ƶ������ʵ���=1.5����4-0��=6mol����ȷ�𰸣�KNO3��S��6��
������������,��������Ӿ���ǿ������,������Cu����ͭ����,��������ԭ����NO2,���ӷ���ʽΪCu+4H++2NO3-=Cu2++2NO2��+2H2O����������ǿ������,������������������S����,������Һ����ǣ��������������ữ����������Һ����,����Һ�м������������ữ����������Һ,����а�ɫ��������˵���������ӣ���ȷ�𰸣�Cu+4H++2NO3-=Cu2++2NO2��+2H2O�� S������Һ�м������������ữ����������Һ,����а�ɫ��������˵���������ӡ�
��2�����������ײ�����������ұ�ը,�䱬ը������4��,2�ֲ����ǿ����е���Ҫ�ɷ�Ϊ����������,��һ�����������ʹʪ�����ɫʯ����ֽ���,Ϊ����,����ԭ���غ�֪������ˮ����,��Ӧ����ʽΪ:![]() ����ȷ����
����ȷ����![]() ��
��
��3�� N4H4��SO4��2Ϊ������ˮ��ǿ�����,���ռ������N4����,�����ӽ����������������N4�����ˮ,��Ӧ�����ӷ���ʽΪ:N4H44++4OH-= N4��+4H2O����ȷ����N4H44++4OH-= N4��+4H2O��


 Ӧ����㲦ϵ�д�
Ӧ����㲦ϵ�д� ״Ԫ����ϵ�д�
״Ԫ����ϵ�д� ͬ������ϵ�д�
ͬ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и��������У���ѧ�����Ͳ�ͬ���� ( )
A. NaCl��CaCl2 B. H2O��NH3 C. H2SO4��CsCl D. SiCl4��CH4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͭ���ǵ��������¿�ѧ�������ܺϳɵ�һ�����ʡ�Ȼ�����ڷ��֣��ҹ��س�����ٸ�õ�һ�����Ͼ��ǹ���ͭ�������й��ڹ���ͭ����˵��������ǣ� ��
A. ������B. ������ˮC. ���ڹ�����D. ������ˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������Ӱ�����ǵ������뽡����ij�����������п��ܺ������¿����������ӣ�Na+��NH4+��Mg2+��Al3+��SO42����NO3����Cl����ijͬѧ�ռ��˸õ���������������Ҫ��Ԥ������������Һ����Ʋ��������ͼ��ʵ�飺

�������ϵ�ʵ�����������ͬѧ�ó��Ľ��۲���ȷ���ǣ�������
A. �����п϶�����NH4+��Mg2+��SO42����NO3��
B. �����п��ܴ���Na+��Cl��
C. ������һ������Al3+
D. �������п��ܴ���NaNO3��NH4Cl��MgSO4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�� A��B��C��D��E��ͬһ���ڵ���������Ԫ�أ�A��B������������Ӧ��ˮ������ʼ��ԣ��Ҽ���B��A��C��D����̬�⻯����ȶ���C��D��E��������Ԫ����ԭ�Ӱ뾶��С��Ԫ�أ������ǵ�ԭ��������С�����˳����
A. A��B��C��D��E B. E��C��D��B��A
C. B��A��D��C��E D. C��D��A��B��E
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʼ��ܸ����ᷴӦ�����ܸ�����������Һ��Ӧ���ǣ� ��
�� NaHCO3 �� Al2O3 �� Al(OH)3 �� Al
A.�ۺ͢�B.�٢ڢ�C.�ڢۢ�D.�٢ڢۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ӻ������Ӷ�Ϊϡ������Ԫ��ԭ�ӽṹ���������ӱ����������������Ӳ�����ӻ������ǣ� ��
A. MgCl2B. BaF2C. NaBrD. NaI
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������AG��ʾ��Һ����ȣ������ʽΪ��![]() �������£�ʵ��������0.1mol/L��������Һ�ζ�10mL 0.1mol/L MOH��Һ���ζ���������ͼ��ʾ������˵����ȷ����
�������£�ʵ��������0.1mol/L��������Һ�ζ�10mL 0.1mol/L MOH��Һ���ζ���������ͼ��ʾ������˵����ȷ����
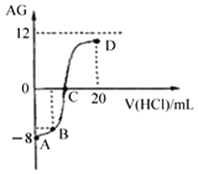
A. �õζ����̿�ѡ���̪��Ϊָʾ��
B. C��ʱ����������Һ���������10 mL
C. ��Һ����ˮ�����c(H+)��C��>D��
D. ��B������������Һ���Ϊ5 mL��������Һ�У�c(M+)+c(H+)= c(MOH)+ c(OH-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�о���ѧϰС���������ͼװ����ȡ����֤SO2�����ʡ�

��ش�
��1��д��A��Ӧװ���еĻ�ѧ����ʽ��____________
��2��������NaOH��Һ��������________________
��3��Ϊ����֤SO2�����������ϴ��ƿ���п�ѡ����Լ���_________��
A������ʯ��ˮ B����ɫ��̪��Һ C����ˮ D����ɫʯ����Һ
��4������˵����ȷ����____________��
A������װ���м����Լ���ҩƷ�����ٽ��������Լ��
B��ʵ�鿪ʼʱ��ֻ���Һ©��������������ʹҺ��˳������
C��ʵ�鿪ʼ��ϴ��ƿ����������Һ����ɫ�����߾���֤��SO2����Ư����
D��ʵ�鿪ʼ��ϴ��ƿ���пɹ۲쵽��ɫ�����������������˵��SO2���л�ԭ��
��5��д��ϴ��ƿ���з�Ӧ�Ļ�ѧ����ʽ��_____________
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com