
| A. | 为了防止白色污染应回收废旧塑料并加以焚烧 | |
| B. | 手机壳上贴的碳纤维膜是一种新型无机非金属材料 | |
| C. | 当今雾霾天气频发是由于人类活动对自然环境的影响所造成的 | |
| D. | 离子交换膜在工业上应用广泛,在氯碱工业中使用阳离子交换膜 |
分析 A.焚烧塑料可导致环境污染;
B.碳纤维属于无机非金属材料;
C.汽车尾气为导致雾霾的主要原因;
D.氯碱工业中氯离子放电,阳离子需要移动到阴极.
解答 解:A.焚烧废旧塑料,会导致大气污染,不利于环境保护,故A错误;
B.碳纤维属于无机非金属材料,是一种新型无机非金属材料,故B正确;
C.汽车尾气为导致雾霾的主要原因,是由于人类活动对自然环境的影响所造成的,故C正确;
D.氯碱工业中氯离子放电,阳离子需要移动到阴极,则用阳离子交换膜,故D正确.
故选A.
点评 本题考查物质的性质与用途,为高频考点,把握物质的性质、发生的反应、性质与用途的关系为解答的关键,侧重分析与应用能力的考查,注意化学与生活、生产的联系,题目难度不大.


科目:高中化学 来源: 题型:实验题
 催化还原CO2是解决温室效应及能源问题的重要手段之一.研究表明,在Cu/ZnO催化剂存在下,CO2和H2可发生两个反应,分别生成CH3OH和CO.反应的热化学方程式如下:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H1=-53.7kJ•mol-1 I CO2(g)+H2(g)?CO(g)+H2O(g)△H2Ⅱ
催化还原CO2是解决温室效应及能源问题的重要手段之一.研究表明,在Cu/ZnO催化剂存在下,CO2和H2可发生两个反应,分别生成CH3OH和CO.反应的热化学方程式如下:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H1=-53.7kJ•mol-1 I CO2(g)+H2(g)?CO(g)+H2O(g)△H2Ⅱ| T(K) | 催化剂 | CO2转化率(%) | 甲醇选择性(%) |
| 543 | Cat.1 | 12.3 | 42.3 |
| 543 | Cat.2 | 10.9 | 72.7 |
| 553 | Cat.1 | 15.3 | 39.1 |
| 553 | Cat.2 | 12.0 | 71.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
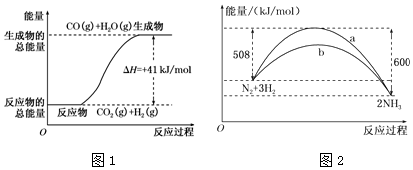
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
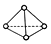 ,它是一种非极性分子.(填“极性”或“非极性”)
,它是一种非极性分子.(填“极性”或“非极性”)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯的实验式:H2C═CH2 | B. | 四氯化碳的电子式: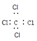 | ||
| C. | 含10个中子的氧原子:${\;}_{8}^{18}$O | D. | Al3+的结构示意图: |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
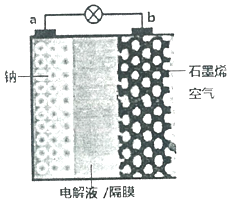 继锂电池之后,近几年科学家又研制出稳定性更高、电压损失更小的“钠--空气电池”.其反应原理是:2Na+O2=Na2O2,装置如图,其中电解液为NaPF6,可传导Na+.电池放电时,下列说法不正确的是( )
继锂电池之后,近几年科学家又研制出稳定性更高、电压损失更小的“钠--空气电池”.其反应原理是:2Na+O2=Na2O2,装置如图,其中电解液为NaPF6,可传导Na+.电池放电时,下列说法不正确的是( )| A. | a电极为负极 | |
| B. | Na+向b极移动 | |
| C. | a极发生氧化反应 | |
| D. | b电极的电极反应式:O2+2Na++4e-═Na2O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
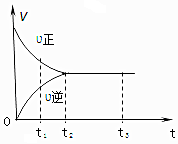 如图是可逆反应:X2+3Y2?2Z2在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述正确的是( )
如图是可逆反应:X2+3Y2?2Z2在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述正确的是( )| A. | t1时,反应只向正方向进行 | B. | t2时,反应未达到限度 | ||
| C. | t2~t3,反应已停止进行 | D. | t2~t3,各物质的浓度不再发生变化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com