
判断下列离子方程式是否正确,正确的打“√”错误的打“×”,并写出正确的离子方程式.
①钛粉溶于稀盐酸中:2Fe+6H+═2Fe3++3H2↑
②用三氯化铝溶液和氨水制Al(OH)3沉淀:Al3++3H2O═Al(OH)3↓+3H+
③氢氧化铁溶于盐酸:OH﹣+H+═H2O
④氢氧化钡溶液与硫酸铜溶液混合:2OH﹣+Cu2+═Cu(OH)2↓
⑤二氧化硫气体通入氢氧化钠溶液中:SO2+2OH﹣═SO42﹣+H2O .
考点: 离子方程式的书写.
分析: ①铁与盐酸反应生成氯化亚铁和氢气,不会生成铁离子;
②氨水为弱碱,一水合氨在离子方程式中应该保留分子式;
③氢氧化铁为难溶物,离子方程式中不能拆开;
④氢氧化钡与硫酸铜反应生成硫酸钡沉淀和氢氧化铜沉淀,漏掉了生成硫酸钡的反应;
⑤二氧化硫与氢氧化钠溶液反应生成亚硫酸钠和水.
解答: 解:①铁与盐酸反应生成氯化亚铁和氢气,离子方程式为:Fe+2H+═Fe2++H2↑,故(1)错误;原因:不符合反应的客观事实;
故答案为:×,Fe+2H+═Fe2++H2↑;
②一水合氨为弱电解质,离子方程式中不能拆开,正确的离子方程式为:Al3++3NH3•H2O=Al(OH)3↓+3NH4+,
故答案为:×,Al3++3NH3•H2O=Al(OH)3↓+3NH4+;
③氢氧化铁不能拆开,正确的离子方程式为:Fe(OH)3+3H+=Fe3++3H2O,
故答案为:×,Fe(OH)3+3H+=Fe3++3H2O;
④漏掉了钡离子与硫酸根离子的反应,正确的离子方程式为:SO42﹣+Ba2++Cu2++2OH﹣=Cu(OH)2↓+BaSO4↓,
故答案为:×,SO42﹣+Ba2++Cu2++2OH﹣=Cu(OH)2↓+BaSO4↓;
⑤氢氧化钠溶液与二氧化硫反应生成亚硫酸钠,不是生成硫酸钠,正确的离子方程式为:SO2+2OH﹣═SO32﹣+H2O,
故答案为:×,SO2+2OH﹣═SO32﹣+H2O.
点评: 本题考查了离子方程式的正误判断,为中等难度的试题,注意明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)、检查是否符合原化学方程式等.


 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案科目:高中化学 来源: 题型:
把SO2通入Fe(NO3)3溶液中,溶液由黄色变为浅绿色,但立即又变为黄色,此时若滴入BaCl2溶液,则会产生白色沉淀.在上述一系列变化过程中,最终被还原的是()
A. SO2 B. NO3﹣ C. Fe3+ D. Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:
一定量CO2通入某浓度的NaOH溶液得溶液A,向A溶液中逐滴滴入稀盐酸,加入n(HCl)与生成nCO2的关系如图.下列有关叙述正确的是( )
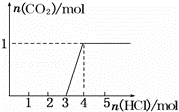
|
| A. | 通入的CO2气体在标准状况下可能大于22.4L |
|
| B. | A溶液中n(NaOH)=2n(Na2CO3) |
|
| C. | A溶液中既含Na2CO3,又有NaHCO3 |
|
| D. | A溶液中一定只有Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
能用OH﹣+H+═H2O 这个离子方程式表示的化学反应的是()
A. 氢氧化铝和硝酸溶液反应 B. Fe(OH)3溶液和硫酸反应
C. 氢氧化钡溶液和稀硫酸 D. KOH溶液和稀硝酸反应
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关化学用语表示正确的是( )
|
| A. | 乙炔的电子式H:C:::C:H | B. |
|
|
| C. | 对甲基苯甲醇的结构简式: | D. | 乙醇分子的比例模型: |
查看答案和解析>>
科目:高中化学 来源: 题型:
某有机物的结构简式为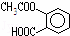 ,它可以发生的反应类型有( )
,它可以发生的反应类型有( )
①取代 ②加成 ③消去 ④酯化 ⑤水解 ⑥中和 ⑦缩聚 ⑧加聚.
|
| A. | 只有①②④⑤ | B. | 只有①②④⑤⑥ | C. | 只有①②④⑤⑥⑦ | D. | 只有①②④⑤⑥⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:
为测定某有机化合物X的结构,进行如下实验:
(1)取一定量有机物X在氧气中完全燃烧,测得生成8.8g CO2和3.6g H2O,消耗标准状况下的氧气5.6L,则X中含有 种元素.
(2)用质谱仪测得A的相对分子质量为44,则X的分子式为 .
(3)根据价键理论,试写出X可能的结构简式(不考虑含有 结构的物质) .
结构的物质) .
(4)X的核磁共振氢谱中出现两个不同位置的峰,则X与氢气反应的化学方程式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
将30mL 0.5mol/L NaOH 溶液加水稀释到500mL,稀释后溶液中NaOH的物质的量浓度为()
A. 0.3 mol/L B. 0.03 mol/L C. 0.05 mol/L D. 0.04 mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com