
| A. | 35 Cl和37 Cl | B. | CH3CH2OH和CH3OCH3 | ||
| C. | CH3CH3和CH3CH2CH3 | D. | H2O和H2O2 |
分析 同分异构体是指分子式相同,但结构不同的化合物;
结构相似、分子组成相差若干个“CH2”原子团的有机化合物互相称为同系物;
同位素是质子数相同,而中子数不同的原子;据此解答即可.
解答 解:A、35Cl和37Cl质子数相同,中子数不同,两者互为同位素,故A错误;
B、CH3CH2OH和CH3OCH3两者分子式相同,结构不同,互为同分异构体,故B正确;
C、CH3CH3和CH3CH2CH3两者结构相似,分子组成上相差1个“CH2”原子团,互为同系物,故C错误;
D、H2O和H2O2分别为H和O两种元素构成的不同种化合物,故D错误,故选B.
点评 本题主要考查了同分异构体、同素异形体、同位素、同一物质等知识,根据概念即可解答.


科目:高中化学 来源: 题型:选择题
| A. | 只有①②③⑤ | B. | 只有①④⑤ | C. | 只有①③④⑤ | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
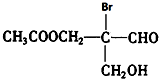 凡有一个手性碳原子的物质具有光学活性,如图物质有光学活性,发生下列反应后生成的有机物仍有光学活性的是( )
凡有一个手性碳原子的物质具有光学活性,如图物质有光学活性,发生下列反应后生成的有机物仍有光学活性的是( )| A. | 与乙酸发生酯化反应 | B. | 与NaOH水溶液共热 | ||
| C. | 与银氨溶液作用发生银镜反应 | D. | 催化剂作用下与H2作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
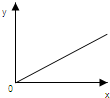
| A. | 一定状况下,气体摩尔体积(y)与该气体的物质的量(x)的关系 | |
| B. | 铁在氯气中燃烧,生成FeCl3的物质的量(y)与消耗氯气的物质的量(x)的关系 | |
| C. | 将铁在常温下放入浓硫酸中,生成气体的物质的量(y)与消耗浓硫酸的物质的量(x)的关系 | |
| D. | H2SO4溶液的物质的量浓度(y)与其质量分数(x) 的关系 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2Na2O2+2CO2=2Na2CO3+O2 | B. | Na2O+CO2=Na2CO3 | ||
| C. | 2NaOH+CO2=Na2CO3+H2O | D. | 2NaHCO3 $\frac{\underline{\;\;△\;\;}}{\;}$ Na2CO3+CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 从C(s,石墨)═C(s,金刚石)△H=+1.9 kJ•mol-1,可知石墨比金刚石更稳定 | |
| B. | 等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量更多 | |
| C. | 由H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ•mol-1,可知含1 mol CH3COOH的溶液与含1 mol NaOH的溶液充分混合反应,放出的热量等于57.3 kJ | |
| D. | 2g H2完全燃烧生成液态水放出285.8 kJ热量,则氢气燃烧的热化学方程式为2H2(g)+O2(g)═2H2O(l)△H=+571.6 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com