
����Ŀ��ijͬѧȡһ�������������Ͻ���100 mLxmol/Lϡ�����ַ�Ӧ����Ӧ������û������ų����ڷ�Ӧ���������Һ�У���μ���2 mol/L NaOH��Һ������ NaOH��Һ�����(mL)��������������ʵ���(mol)�Ĺ�ϵ��ͼ��ʾ��
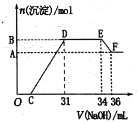
(1)д��EF�η�����Ӧ�����ӷ���ʽ____________
(2)C���Ӧ����Һ�к��е������ӳ�Na+�⣬������_______��
(3)x =________��
(4)�����Ͻ����������ʵ�������Ϊ_________��
���𰸡�Al��OH��3+OH-=AlO2-+2H2O NH4+��Al3+��Fe3+ 0.74 25%
��������
���ۺ����۵Ļ������100mLxmol/LϡHNO3��ַ�Ӧ��������ΪAl3+��Fe3+��ͨ�����⣬��Ӧ������û������ų���˵��û�е������������ɣ����ͼ��NԪ����+5�����-3�ۣ�������笠����ӡ���ͼ�ɵ������������������������ҺӦ�������ᷴӦ�������ɳ�������������ȫ����ͼ֪������������������Һ�����������䣬����������NH4+�����˷�Ӧ��������NaOH�ĵμӣ������ķ�Ӧ�����У�H++OH-=H2O��Fe3++3OH-=Fe(OH)3����Al3++3OH-=Al(OH)3����NH4++OH-�TNH3H2O��Al(OH)3+OH-=AlO2-+2H2O���ݴ˷������
(1)E��F֮������������٣�����ΪAl(OH)3�ܹ�������������Һ���ܽ⣬��Ӧ�����ӷ���ʽΪAl(OH)3+OH-=AlO2-+2H2O���ʴ�Ϊ��Al(OH)3+OH-=AlO2-+2H2O��
(2)���ۺ����۵Ļ������һ����ϡHNO3��ַ�Ӧ��������ΪAl3+��Fe3+��ͨ�����⣬��Ӧʼ��û���������ɣ���ͼ�ɵ������������������������ҺӦ�������ᷴӦ������C�㺬��Na+����������ȫ����ͼ֪������������������Һ�����������䣬Ϊ����������NH4+�����˷�Ӧ��NH4++OH-�TNH3H2O��������Һ�д���NH4+����C���Ӧ����Һ�к��е������ӳ�Na+�⣬������NH4+��Al3+��Fe3+���ʴ�Ϊ��NH4+��Al3+��Fe3+��
(3)E��F֮������������٣�ΪAl(OH)3�ܽ�������������Һ�У�
�䷴Ӧ�ķ���ʽΪAl(OH)3+NaOH=NaAlO2+2H2O�����������������������ʵ���֮��Ϊ1��1��EF�ε�n(NaOH)=2mol/L��(36-34)��10-3L=0.004mol������Al��Al(OH)3��NaOH��NaAlO2���������ʵ���Ϊ0.004mol�����������ᷴӦû�����������˵����ԭ����Ϊ����泥�DE��ΪNH4NO3��NaOH��Ӧ������NH4NO3��NaOH��n(NH4NO3)=n(NaOH)=(34-31)��10-3L��2mol/L=0.006mol������E��ʱ����Һ�е������������ƺͰ�ˮ��n(NH3H2O )=n(NH4+)=0.006mol��n(NaNO3)=n(NaOH)=34��10-3L��2mol/L=0.068mol�����ݵ�ԭ���غ�֪��c(HNO3)=![]() =
=![]() =0.74mol/L���ʴ�Ϊ��0.74��
=0.74mol/L���ʴ�Ϊ��0.74��
(4)��������ʼ�����ᷴӦ��ʱ������+3�����ӣ�NԪ�ر��笠����ӡ�������ymol��
Al����Ϊ0.004mol��NH4+Ϊ0.006mol�����ݵ�ʧ�����غ㣺3y+0.004��3=0.006��8����ã�y=0.012mol������������Ϊ0.012mol������ԭ���غ�֪���������ʵ�����0.012mol�������Ͻ����������ʵ�������Ϊ![]() ��100%=25%���ʴ�Ϊ��25%��
��100%=25%���ʴ�Ϊ��25%��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��CO2�Ļ����������ǿ�ѧ���о����ȵ���⣬������CH4��CO2�Ʊ����ϳ�����(CO��H2)�������Ʊ��״��������ѡ���̼ϩ����ȼ�ϲ�Ʒ��
I.�ƺϳ���
��ѧ������Ʊ������ϳ�������Ӧ���̷�������
��Ӧ��: CH4(g)C(ads)+2H2(g) (����Ӧ)
��Ӧ��:C(ads)+CO2(g)2CO(g) (�췴Ӧ)
������Ӧ��C(ads)Ϊ�����Ի���̿����Ӧ���̵������仯����ͼ��
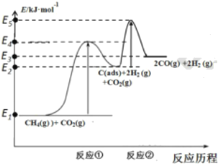
(1) CH4��CO2�Ʊ����ϳ��������Ȼ�ѧ����ʽΪ____�� �����仯ͼ�У�E5+E1_______E4+ E2(����>�� �� ��< �� �� ��= ��)��
II.�״��ϳ�
��ij CO �������Ƽ״��ķ�Ӧ��ϵ�У���������Ҫ��Ӧ�У�
i. CO2(g) + 3 H2(g)CH3OH(g)+H2O(g)��H1< 0
ii.CO2(g) + H2(g)CO (g)+H2O(g) ��H2>0
iii . CO(g)+2H2( g)CH3OH(g) (g) ��H3< 0
(2)5MPa ʱ����ij�ܱ������а�Ͷ�ϱ�n(H2) :n ( CO2) =3:1 ����H2��CO2����Ӧ�ﵽƽ��ʱ�� ��ø���ֵ����ʵ����������¶ȱ仯��������ͼ��ʾ��
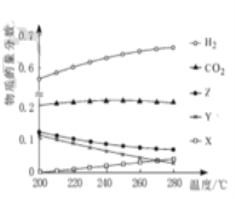
����ϵ��CO2�����ʵ����������¶ȵ�Ӱ�첻�� ԭ����_____��
��250��Cʱ����Ӧ i i ��ƽ�ⳣ��____1(����> ����< ������=��)
�����д�ʩ�У�����״����ʵ���____(����)��
A����������CO B������ѹǿ C��ѭ������ԭ���� D�������¶�
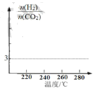
������ͼ�л���n(H2)/ n(CO2)���¶ȱ仯����ͼ_____��
(3)��Ӧi���ܵķ�Ӧ��������ͼ��ʾ��
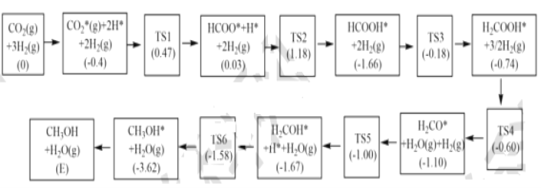
ע�������ڰ��������༰��Ŀ���������������(����������ֻ���ĸ����λ��eV)������TS��ʾ����̬��*��ʾ�����ڴ����ϵ�������Ӧ�����У����ɼ״��ľ��ٲ���ķ�Ӧ����ʽΪ__��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ȼ��ˮ���������Ʊ�H2�ķ�ӦΪ![]()
![]() ÿ��ֻ�ı�һ������(X)�������������䣬CH4��ƽ��ת����
ÿ��ֻ�ı�һ������(X)�������������䣬CH4��ƽ��ת����![]() ��X�ı仯������ͼ��ʾ������˵����ȷ����
��X�ı仯������ͼ��ʾ������˵����ȷ����
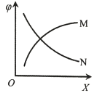
A.ij�����£���CH4(g)��H2O(g)��ʼŨ�Ⱦ�Ϊ0.2 mol/L��![]() = 25%����K=3
= 25%����K=3
B.XΪͶ�ϱ�![]() ʱ��
ʱ��![]() �ı仯����Ϊ����N
�ı仯����Ϊ����N
C.XΪѹǿʱ��![]() �ı仯����Ϊ����M
�ı仯����Ϊ����M
D.XΪ�¶�ʱ��![]() �ı仯����Ϊ����N
�ı仯����Ϊ����N
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����С���о���������A12O3�ĺ������������ϵ�֪�����������Ҫ�ɷ���A12O3 ,������Fe2O3��SiO2�ȡ�������������ȡA12O3�Ĺ������£�
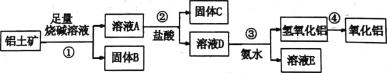
(1)�����������������м��������ռ���Һ����ַ�Ӧ��������Ӧ�����ӷ���ʽ��:______��
(2)�������õ��ķ��뷽����_______��
(3)�������������ѡ����������������Ҫ������_____________(����ĸ)
A.������ B.������ C.������ E.�ƾ��� F.����
(4)��ʵ����������ù���ȷ����������С�鷢�������������������������ԭ������������ȣ������������A12O3 ����������__________(�������һλС������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����С������ʯ�ͷ����Ʒ�ϳ�һ���������ϵ�����ͼ���¡�

��֪X������̼��������Ϊ24��5��X�ж����ѽⷽʽ������A��E����X���ѽ����Ҷ���Ϊͬϵ�D�뱥��NaHCO3��Һ��Ӧ�������塣
��Ϣ��ʾ��±������ǿ��ˮ��Һ�з���ˮ�⣨ȡ������Ӧ���ɴ����磺R-CH2CH2Cl![]() RCH2CH2OH+HCl(ˮ�ⷴӦ)
RCH2CH2OH+HCl(ˮ�ⷴӦ)
��1��C�й����ŵ�����Ϊ______________��
��2����д��X��ֱ���ṹ��ʽ______________��
��3������˵����ȷ����______________��
A�����ý����Ƽ���B��G
B��E��һ�����������Ȼ��ⷢ���ӳɷ�Ӧ�IJ�����2��
C��D��G��1��1��Ӧ�����ɷ���ʽΪC5H10O2���л���
D��E��F�ķ�Ӧ����Ϊȡ����Ӧ
��4����д��A��B�ķ�Ӧ______________��
��5��B��D��Ũ�������������ɼף�д�����ͬ����ͬ���칹��Ľṹ��ʽ______________���������ף���
��6��д���Ļ�ѧ��Ӧ����ʽ______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ѡ�95%�Ҵ����ݶ��ٸ�Ҷ���õ���ȡҺ�����������ԭ��ֲ�Ʒ���ֹ����������£�����˵���������
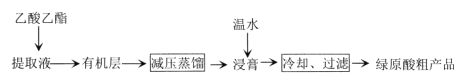
A.�����£���ԭ��������ˮ
B.�������Ҫ�ɷ�����ԭ��
C.��ѹ�����Ŀ���ǽ��������¶ȣ�������ԭ�����
D.��ԭ��ֲ�Ʒ����ͨ���ؽᾧ��һ���ᴿ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪���ֱ�������þ��1��6 g�������������ᷴӦ���ڱ�״��������H21��12 L���ڸ����ᷴӦǰ��������þ�� ( )
A.1��2 gB.0��64 gC.0��4 gD.0��24 g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʾ��ͼ���Ӧ�ķ�Ӧ�����ȷ������������
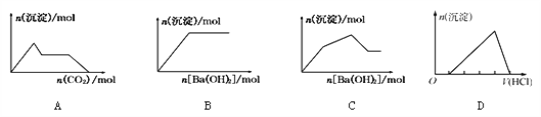
A. ��0.01 mol NaOH��0.01 mol Ba��OH��2�Ļ����Һ�л���ͨ��CO2
B. KHCO3��Һ����μ���Ba��OH��2��Һ
C. KAl��SO4��2��Һ����μ���Ba��OH��2��Һ
D. ���������������Ƶ�ƫ��������Һ�еμ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���10 mL 0.1000 mol��L-1 NaOH��Һ����μ���0.1000 mol��L-1 ��ijһԪ��HX����ҺpH�仯������ͼ������˵������ȷ����

A.��Ũ�ȵ� HX��NaX �����Һ�У�HX�ĵ���̶ȴ���X- ��ˮ��̶�
B.c����ʾ��Һ�д��ڣ�2c(H+) - 2c(OH-) = c(X-) - c(HX)
C.a��b��c����ʾ��Һ�У���ˮ������� c(H+)��c(OH-) ֵ����
D.a ��c����ʾ��Һ�У�c(X-) + c(HX) + c(Na+) = 0.1000 mol��L-1 ʼ�ճ���
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com