
A、漂白粉溶液在空气中失效:ClO-+CO2+H2O═HClO+HCO
| ||||
B、用浓盐酸与MnO2反应制取少量氯气:MnO2+2H++2Cl-
| ||||
| C、NaOH溶液不能保存在玻璃塞的试剂瓶中:SiO2+2OH-=SiO32-+H2O | ||||
| D、向滴有酚酞的氨水中加入盐酸,红色逐渐褪去:H++OH-=H2O |
| ||


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、维生素C具有还原性 |
| B、维生素C具有氧化性 |
| C、该反应中+5价砷被氧化 |
| D、砒霜中毒后可服用维生素C解毒 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na2CO3:CO32-+2H2O?H2O+CO2↑+2OH- |
| B、NH4NO3:NH4++H2O?NH3?H2O+H+ |
| C、CuSO4:Cu2++2H2O?Cu(OH)2↓+2H+ |
| D、KF:F-+H2O→HF+OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H2S?2H++S2- |
| B、HClO=H++ClO- |
| C、CH3COONa=Na++CH3COO- |
| D、NaHCO3?Na++HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氢氧化铁溶于氢碘酸中:2Fe(OH)3+6H++2I-=2Fe2++I2+6H2O |
| B、明矾溶液中加入氢氧化钡溶液,使其产生沉淀的物质的量达最大值:Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+AlO2-+2H2O |
| C、Mg(HCO3)2溶液中加入过量石灰水:Mg2++2HCO3-+2Ca2++4OH-=2CaCO3↓+2H2O+Mg(OH)2↓ |
| D、向100mL 0.1mol/L的FeBr2溶液中通入0.012mol Cl2:10Fe2++14Br-+12Cl2=10Fe3++7Br2+24Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、22.4LNe含有NA个Ne分子 |
| B、1.7 g氨气所含有的电子数目为10NA |
| C、在H2O2+Cl2=2HCl+O2反应中,每生成32g氧气,则转移NA个电子 |
| D、常温常压下,16g O3含有的氧原子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
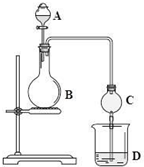 化学实验中,同一个装置可以用于不同的实验,例如图中的实验装置.(如图所示,B中可为固体或液体,可加热)
化学实验中,同一个装置可以用于不同的实验,例如图中的实验装置.(如图所示,B中可为固体或液体,可加热)查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com