

分析 (1)由于NaCl的溶解度受温度的影响变化不大,因此从氯化钠溶液中得到氯化钠固体,选择蒸发溶剂法获得;除去自来水中的Cl-等杂质,获得纯净的水,可以可以水的沸点低,而NaCl的沸点高,用蒸馏的方法获得蒸馏水;由于碘单质在水中的溶解度比在有机物苯中小,水与苯互不相溶,碘与苯不能发生反应,可以用苯作萃取剂,采用萃取的方法分离获得,因此从碘水中分离出I2,该分离方法的名称为萃取;
(2)装置A中①的名称是蒸馏烧瓶;
(3)实验室中制取的Fe(OH)3胶体中常常含有杂质Cl-离子,可以利用胶体的分散质微粒足记介于1nm-100nm之间,不能透过半透膜而Cl-可以透过半透膜的性质,用渗析的方法除去Fe(OH)3胶体中混有的杂质Cl-离子.
解答 解:(1)由于NaCl的溶解度受温度的影响变化不大,因此从氯化钠溶液中得到氯化钠固体,选择蒸发溶剂法获得,应该选择的实验装置是D;除去自来水中的Cl-等杂质,获得纯净的水,可以可以水的沸点低,而NaCl的沸点高,用蒸馏的方法获得蒸馏水,选择装置是A;由于碘单质在水中的溶解度比在有机物苯中小,水与苯互不相溶,碘与苯不能发生反应,可以用苯作萃取剂,采用萃取的方法分离获得,因此从碘水中分离出I2,选择装置B,该分离方法的名称为萃取,
故答案为:D;A;B;萃取;
(2)装置A中①的名称是蒸馏烧瓶,故答案为:蒸馏烧瓶;
(3)实验室中制取的Fe(OH)3胶体中常常含有杂质Cl-离子,可以利用胶体的分散质微粒足记介于1nm-100nm之间,不能透过半透膜而Cl-可以透过半透膜的性质,用渗析的方法除去Fe(OH)3胶体中混有的杂质Cl-离子,故答案为:渗析.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、性质差异及混合物分离方法为解答的关键,侧重分析与应用能力的考查,题目难度中等.


 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素原子第一电离能大小关系:Z>Y>W>X>M | |
| B. | XZ2、X2M2、W2Z2均为直线形的共价化合物 | |
| C. | Y与M形成化合物键长大于Z与M形成化合物的键长 | |
| D. | 由X、Y、Z、M四种元素形成的化合物一定既有离子键,又有共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4LH2含有的分子数为1NA | |
| B. | 常温常压下,1.06gNa2CO3含有的Na+数为0.02NA | |
| C. | 标准状况下,1NACO2分子占有的体积为22.4L | |
| D. | 物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl-个数为1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
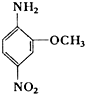 2-氨基-5-硝基苯甲醚俗称红色基B,其结构简式如右所示.若化学式与红色基B相同,且氨基与硝基直接连在苯环上并呈对位时的同分异构体数目(不包括红色基B)可能为( )
2-氨基-5-硝基苯甲醚俗称红色基B,其结构简式如右所示.若化学式与红色基B相同,且氨基与硝基直接连在苯环上并呈对位时的同分异构体数目(不包括红色基B)可能为( )| A. | 6种 | B. | 7种 | C. | 9种 | D. | 10种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com