
【题目】氧化还原反应的实质是
A.化合价的升降B.分子中各原子重新组合
C.电子的得失或偏移D.氧原子的得失
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:高中化学 来源: 题型:
【题目】下列除杂操作可行的是
A.通过浓硫酸除去HCl中的H2OB.通过灼热的CuO除去H2中的CO
C.通过灼热的镁粉除去N2中的O2D.通过水除去CO中的CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的数值,下列说法正确的是( )
A. 1molCnH2n+2中有3nNA 对共用电子 B. 在18gD2O中含有10NA个质子
C. 1molCH2Cl2在标准状况下约为22.4L D. 1molNa2O2中阴阳离子个数比为1:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用氯酸钾和二氧化锰制取氧气的反应方程式为:2KClO3 ![]() 2KCl+3O2↑
2KCl+3O2↑
回答下列问题:
(1)该反应中被氧化的元素名称为 , 生成1mol O2时转移电子的数目是 .
(2)从反应后的固体混合物中分离出难溶于水的MnO2的具体实验操作名称: .
(3)分离出的MnO2可用于实验室制取Cl2 , 化学方程式为:MnO2+4HCl(浓) ![]() MnCl2+Cl2↑+2H2O,其离子方程式为 .
MnCl2+Cl2↑+2H2O,其离子方程式为 .
(4)若两个反应中转移的电子的物质的量相同,则生成的O2和Cl2在相同状况下的体积比为
(5)以上两个反应都用到MnO2 , 其作用分别是、 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】砷及其化合物有毒,如砒霜(As2O3)有剧毒,环境监测和法医学分析砒霜中毒的反应原理:
As2O3+6Zn+12HCl=6ZnCl2+2AsH3↑+3H2O
①反应中还原剂是 , 被还原的元素是 , (用化学式回答)若参加反应Zn的质量为19.5g,则生成的气体在标准状况下的体积为L,
②用双线桥法标出上述反应中电子转移的方向和数目.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】砷及其化合物有毒,如砒霜(As2O3)有剧毒,环境监测和法医学分析砒霜中毒的反应原理:
As2O3+6Zn+12HCl=6ZnCl2+2AsH3↑+3H2O
①反应中还原剂是 , 被还原的元素是 , (用化学式回答)若参加反应Zn的质量为19.5g,则生成的气体在标准状况下的体积为L,
②用双线桥法标出上述反应中电子转移的方向和数目.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】重铬酸钾是一种重要的化工原料,一般由铬铁矿制备,铬铁矿的主要成分为FeO·Cr2O3,还含有硅、铝等杂质。制备流程如图所示:
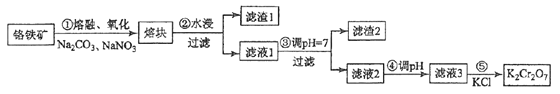
回答下列问题:
(1)步骤①的主要反应为:FeO·Cr2O3+Na2CO3+NaNO3 = Na2CrO4+ Fe2O3+CO2+ NaNO2,上述反应配平后NaNO3与FeO·Cr2O3的系数比为__________。该步骤能否_________(填“能”或“不能”)使用陶瓷容器。
(2)滤渣1中含量最多的金属元素是____________,滤渣2的主要成分是_______________及含硅杂质。
(3)步骤④调滤液2的pH使之变_________ (填“大”或“小”),理由是________(用离子方程式表示)。
(4)有关物质的溶解度如图所示。向“滤液3”中加入适量KCl,蒸发浓缩,冷却结晶,过滤得到K2Cr2O7固体。冷却到10℃得到的K2Cr2O7固体产品最多。
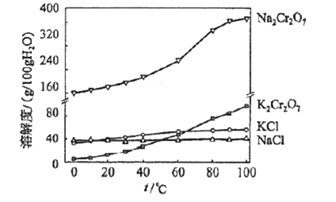
步骤⑤的化学方程式为 _________________。
(5)某工厂用76Kg铬铁矿粉(含Cr2O3 40%)制备K2Cr2O7,最终得到产品41.16Kg, 则产率为_________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com