
 )是一种有机合成中间体,A的合成路线如图所示,其中B~I分别代表一种有机物.
)是一种有机合成中间体,A的合成路线如图所示,其中B~I分别代表一种有机物.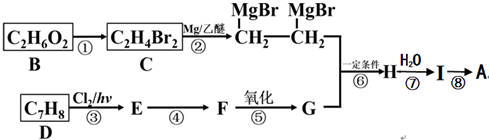
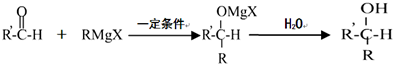
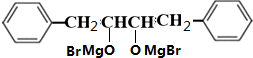 ;
;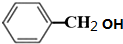 +O2$→_{△}^{铜}$2H2O+2
+O2$→_{△}^{铜}$2H2O+2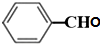 ;
;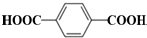 在催化剂的作用下生成聚合物--涤纶,写出涤纶的
在催化剂的作用下生成聚合物--涤纶,写出涤纶的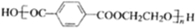 ;
; (任写一种).
(任写一种).分析 根据各物质的转化关系及分子式可知,B为HOCH2CH2OH,B与溴化氢发生取代反应生成C为BrCH2CH2Br,B发生信息中的反应生成MgBrCH2CH2MgBr,根据A的结构可知,I为 ,I发生消去反应生成A,根据题中信息可知,H为
,I发生消去反应生成A,根据题中信息可知,H为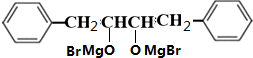 ,根据转化关系,结合D的分子式可知,D为
,根据转化关系,结合D的分子式可知,D为 ,D发生取代反应生成E为
,D发生取代反应生成E为 ,E发生水解生成F为
,E发生水解生成F为 ,F发生氧化得G为
,F发生氧化得G为 ,据此答题.
,据此答题.
解答 解:根据各物质的转化关系及分子式可知,B为HOCH2CH2OH,B与溴化氢发生取代反应生成C为BrCH2CH2Br,B发生信息中的反应生成MgBrCH2CH2MgBr,根据A的结构可知,I为 ,I发生消去反应生成A,根据题中信息可知,H为
,I发生消去反应生成A,根据题中信息可知,H为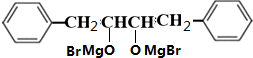 ,根据转化关系,结合D的分子式可知,D为
,根据转化关系,结合D的分子式可知,D为 ,D发生取代反应生成E为
,D发生取代反应生成E为 ,E发生水解生成F为
,E发生水解生成F为 ,F发生氧化得G为
,F发生氧化得G为 ,
,
(1)D为 ,D的名称是 甲苯,根据上面的分析可知,第⑧步反应的类型是消去反应,
,D的名称是 甲苯,根据上面的分析可知,第⑧步反应的类型是消去反应,
故答案为:甲苯; 消去反应;
(2)第④步是卤代烃的碱性水解,所以的反应条件是氢氧化钠水溶液、加热,H的结构简式是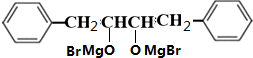 ,
,
故答案为:氢氧化钠水溶液、加热;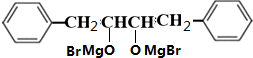 ;
;
(3)第①步反应的化学方程式是HOCH2CH2OH+2HBr$\stackrel{△}{→}$2H2O+BrCH2CH2Br,
故答案为:HOCH2CH2OH+2HBr$\stackrel{△}{→}$2H2O+BrCH2CH2Br;
(4)第⑤步反应的化学方程式是2 +O2$→_{△}^{铜}$2H2O+2
+O2$→_{△}^{铜}$2H2O+2 ,
,
故答案为:2 +O2$→_{△}^{铜}$2H2O+2
+O2$→_{△}^{铜}$2H2O+2 ;
;
(5)B为HOCH2CH2OH,B与 在催化剂的作用下发生缩聚反应生成涤纶的结构简式 为
在催化剂的作用下发生缩聚反应生成涤纶的结构简式 为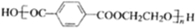 ,
,
故答案为: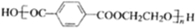 ;
;
(6)I为 ,根据条件①含有2个苯环,②能与FeCl3溶液发生显色反应,说明有酚羟基,③核磁共振氢谱有5个峰,说明有5种位置的氢原子,则符合条件的I的同分异构体的结构简式为
,根据条件①含有2个苯环,②能与FeCl3溶液发生显色反应,说明有酚羟基,③核磁共振氢谱有5个峰,说明有5种位置的氢原子,则符合条件的I的同分异构体的结构简式为 等,
等,
故答案为: .
.
点评 本题考查有机物推断,为高频考点,侧重考查学生判断及知识综合运用能力,需要学生具有扎实的基础知识才能解答,知道常见有机物官能团及其性质、反应类型及反应条件,难点是限制型同分异构体的书写.


科目:高中化学 来源: 题型:选择题
| 物质及变化 | 描述 | 相关知识 | |
| A | 碘化钾溶液滴到土豆片上 | 变蓝色 | 土豆片含淀粉 |
| B | 煤的气化 | 化学变化 | 主要反应是碳与水生成水煤气等 |
| C | 乙烯和苯 | 都能使溴水褪色 | 分子中含有相同的碳碳双键 |
| D | 蔗糖和麦芽糖 | 多糖 | 二者互为同分异构体 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
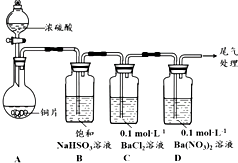
| 序号 | 实验操作 | 实验现象 |
| 1 | 取0.3g 纯净Na2SO3固体,向其中加入10mL2mol•L-1盐酸,再滴入4滴BaCl2溶液 | 产生无色气泡;滴入BaCl2溶液后,开始无现象,4min后,溶液变浑浊 |
| 2 | 取0.3g 纯净Na2SO3固体,向其中加入10mL 2mol•L-1 HNO3,再滴入4滴BaCl2溶液 | 产生无色气泡;滴入BaCl2溶液后,开始无现象,2h后,溶液变浑浊 |
| 3 | 取0.3g 纯净Na2SO3固体,向其中加入10mL 浓HNO3,再滴入4滴BaCl2溶液 | 产生红棕色气体;滴入BaCl2溶液后,溶液立即产生大量白色沉淀 |
| 序号 | 实验操作 | 实验现象 |
| 4 | 取固体混合物,向其中加入10mL2mol•L-1 HNO3,再滴入4滴BaCl2溶液 | 产生无色气泡;滴入BaCl2溶液后,开始无现象,20min后,溶液变浑浊 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 弱酸 | H2CO3 | 水杨酸(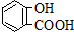 ) ) |
| 电离平衡常数(25℃) | Ka1=4.3×10-7 Ka2=5.6×10-11 | Ka1=1.3×10-3 Ka2=1.1×10-11 |
| A. | 常温下,等浓度、等体积的NaHCO3溶液pH小于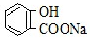 溶液pH 溶液pH | |
| B. | 常温下,等浓度、等体积的Na2CO3溶液和  溶液中所含离子总数前者小于后者 溶液中所含离子总数前者小于后者 | |
| C. |  +2NaHCO3→ +2NaHCO3→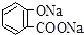 +2H2O+2CO2↑ +2H2O+2CO2↑ | |
| D. |  最多可与2molCO2反应 最多可与2molCO2反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
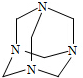
| A. | 1:1 | B. | 3:2 | C. | 2:3 | D. | 2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
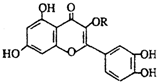 天然维生素P(结构如图)存在于槐树花蕾中,它是一种营养增补剂,关于维生素P的叙述错误的是( )
天然维生素P(结构如图)存在于槐树花蕾中,它是一种营养增补剂,关于维生素P的叙述错误的是( )| A. | 1mol天然维生素P在一定条件下最多与7molH2加成 | |
| B. | 1mol天然维生素P和溴水反应,可消耗6molBr2 | |
| C. | 可用有机溶剂萃取 | |
| D. | 1mol维生素P可以和4mol NaOH反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 制备1mol HRO3转移电子数一定为2NA | |
| B. | R、Z简单离子的还原性:Z(离子)<R(离子) | |
| C. | HZ分子的稳定性大于HR分子 | |
| D. | HRO3与HZ计量数之比为1:5 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com