
| A. | 2H2(g)+O2(g)═2H2O(1)△H=-149.2 kJ/mol | B. | H2(g)+O2(g)═H2O(1)△H=+285.8 kJ/mol | ||
| C. | 2H2(g)+O2(g)═2H2O(g)△H=-571.6kJ/mol | D. | 2H2(g)+O2(g)═2H2O(1)△H=-571.6kJ/mol |
分析 lgH2完全燃烧生成稳定的氧化物,测得放出142.9kJ的热量,则1molH2完全燃烧生成稳定的氧化物,放出热量为142.9kJ×2=285.8 kJ,结合物质的量与热量成正比、放热反应的焓变为负来解答.
解答 解:lgH2完全燃烧生成稳定的氧化物,测得放出142.9kJ的热量,则1molH2完全燃烧生成稳定的氧化物,放出热量为142.9kJ×2=285.8 kJ,水为液态,则表示该反应的热化学方程式为H2(g)+$\frac{1}{2}$O2(g)═H2O(1)△H=-285.8 kJ/mol或2H2(g)+O2(g)═2H2O(1)△H=-571.6kJ/mol,
故选D.
点评 本题考查热化学方程式的书写,为高频考点,把握反应中能量变化、物质的量与热量的关系为解答的关键,侧重分析与应用能力的考查,注意燃烧热的判断,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 物理过程,吸收热量 | B. | 化学过程,吸收热量 | ||
| C. | 物理过程,放出热量 | D. | 化学过程,放出热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
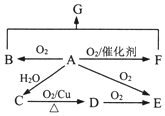 已知A石油裂解的主要产物,相对分子质量为28.B为气体,在标准状况下的密度为1.96g/L.D与F互为同分异构体,F是环状化合物.G的结构简式为:
已知A石油裂解的主要产物,相对分子质量为28.B为气体,在标准状况下的密度为1.96g/L.D与F互为同分异构体,F是环状化合物.G的结构简式为: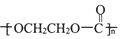 ,在一定条件下,它们有如图转化关系.
,在一定条件下,它们有如图转化关系.
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 活化分子的能量明显增加 | B. | 改变了化学反应的能量变化 | ||
| C. | 降低了反应的活化能 | D. | 增加了活化分子的百分数 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将过量SO2通入稀氨水中:SO2+NH3•H2O═HSO3-+NH4+ | |
| B. | Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+═Fe3++3H2O | |
| C. | 大理石溶于醋酸中:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| D. | AlCl3溶液中加入过量稀氨水:Al3++4NH3•H2O═[Al(OH)4]-+4NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在稀溶液中,H+(aq)+OH-(aq)═H2O(1)△H;若将0.5molH2SO4的浓硫酸与含1 molNaOH的溶液混合的反应热大于△H | |
| B. | (NH4)2CO3(s)═NH4HCO3(s)+NH3(g)△H=+74.9KJ/mol,该反应是吸热反应,因此一定不能自发进行 | |
| C. | 只含NH4+、Cl-、H+、OH-四种离子的溶液中离子浓度可能满足:c(Cl-)>c(H+)>c(NH4+)>c(OH-) | |
| D. | 降低温度和加水稀释,都会使NH4Cl 溶液中c(H+)变小,水解平衡向逆方向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该反应中NH3被还原 | B. | 该反应利用了Cl2的强氧化性 | ||
| C. | 若管道漏气遇氨就会产生白烟 | D. | 生成1mol N2有6mol电子转移 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com