
分析 (1)影响反应速率的因素有:温度、浓度、催化剂、接触面积等;
(2)温度越高反应速率越快,离子浓度越大反应速率越快;
(3)离子浓度越小反应速率越慢.
解答 解:(1)影响该反应速率的因素有:温度、氢离子浓度、催化剂、接触面积等,虽然生成物中有气体,但该反应是在敞口容器中,外界大气压不变,所以氢气压强不影响反应速率,故选①②③;
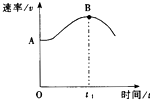
(2)温度越高反应速率越快,离子浓度越大反应速率越快,该反应是放热反应,随着反应的进行,溶液温度升高,溶液中离子浓度降低,但温度影响大于离子浓度影响,所以反应速率加快,故答案为:镁条和盐酸的反应放热,温度升高,反应速率加快;
(3)离子浓度越小反应速率越慢,随着反应的进行,溶液中氢离子浓度降低,虽然溶液温度升高,但离子浓度影响大于温度升高,所以反应速率减慢,
故答案为:反应进行,盐酸浓度减小,反应物浓度减小,反应速率减慢.
点评 本题考查外界影响因素对化学反应速率的影响,侧重考查基本理论,明确外界影响因素及其原理,注意外界因素只是影响因素,起决定性作用的是物质本身性质.


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源:2016-2017学年吉林省长春市高二上学期期初考试化学试卷 题型:选择题
向10mL0. 1mol/LNH4Al(SO4)2溶液中,滴加等浓度Ba(OH)2溶液xmL,下列叙述正确的是
1mol/LNH4Al(SO4)2溶液中,滴加等浓度Ba(OH)2溶液xmL,下列叙述正确的是
A.x=10时,溶液中有NH4+、Al3+、SO42-,且c(NH4+)>c(Al3+)
B.x=15时,溶液中有NH4+、AlO2—、SO42-,且c(NH4+)>2c(SO42-)
C.x=20时,溶液中有Ba2+、AlO2—、OH—,且c(OH—)<c(AlO2—)
D.x=30时,溶液中有Ba2+、Al3+、OH—,且c(OH—)=c(Ba2+)
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ①② | C. | ②③ | D. | 无 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硅便于运输、贮存,从安全角度考虑,硅是最佳的燃料 | |
| B. | 自然界中存在大量的单质硅 | |
| C. | 硅燃烧放出的热量多,且燃烧产物对环境污染程度低,容易有效控制 | |
| D. | 硅常用作太阳能电池的材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ⑤>④>③>②>① | B. | ①>②>③>④>⑤ | C. | ④=⑤>③>①=② | D. | ①=②>③>④=⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 在通常状况下,A为固体单质,如图所示的转化关系,回答:
在通常状况下,A为固体单质,如图所示的转化关系,回答:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ④③②① | B. | ②④③① | C. | ①②③④ | D. | ①②④③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 6:11 | B. | 2:3 | C. | 2:5 | D. | 6:5 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com