

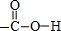
 $\stackrel{②}{→}$
$\stackrel{②}{→}$ $\stackrel{③}{→}$Y$\stackrel{④}{→}$
$\stackrel{③}{→}$Y$\stackrel{④}{→}$
| 反应① | 反应② | 反应③ | |
| 试剂及条件 | |||
| 反应类型 |
 +2NaOH $→_{△}^{醇}$
+2NaOH $→_{△}^{醇}$ 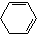 +2NaBr+2H2O
+2NaBr+2H2O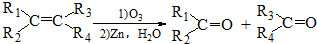 (R1、R2、R3、R4为烃基或H)
(R1、R2、R3、R4为烃基或H)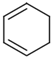 $→_{(2)Zn,H_{2}O}^{(1)O_{3}}$OHC-CH2CH2CHO+OHC-CHO,产物中含氧官能团的名称是醛基,
$→_{(2)Zn,H_{2}O}^{(1)O_{3}}$OHC-CH2CH2CHO+OHC-CHO,产物中含氧官能团的名称是醛基,分析 I.乙烯与溴发生加成反应生成A为BrCH2CH2Br,A发生消去反应生成乙炔,A在氢氧化钠水溶液、加热条件下发生水解反应生成B为HOCH2CH2OH,B发生氧化反应生成C,C与氢气反应又得到B,故B氧化生成C为OHC-CHO,C进一步氧化生成D为HOOC-COOH;
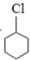
Ⅱ.X与氯气在光照条件下得到一氯环己烷,故X为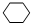 ,一氯环己烷在氢氧化钠醇溶液、加热条件下发生消去反应生成
,一氯环己烷在氢氧化钠醇溶液、加热条件下发生消去反应生成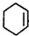 ,环己烯与溴发生加成反应生成Y为
,环己烯与溴发生加成反应生成Y为 ,在氢氧化钠醇溶液、加热条件下发生消去反应生成生成
,在氢氧化钠醇溶液、加热条件下发生消去反应生成生成
(6)由信息可知,
(7)与M互为同分异构体,属于脂肪烃,且分子结构中无支链,核磁共振氢谱显示有四个峰且峰面积之比为1:2:2:3,含有1个甲基,应含有1个碳碳三键、1个碳碳双键.
解答 解:I.乙烯与溴发生加成反应生成A为BrCH2CH2Br,A发生消去反应生成乙炔,A在氢氧化钠水溶液、加热条件下发生水解反应生成B为HOCH2CH2OH,B发生氧化反应生成C,C与氢气反应又得到B,故B氧化生成C为OHC-CHO,C进一步氧化生成D为HOOC-COOH.
(1)D为HOOC-COOH,含有官能团的结构式为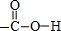 ,故答案为:
,故答案为: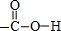 ;
;
(2)①~⑥反应中,①为加成反应,②为取代反应,③为氧化反应,④为加成反应或还原反应,⑤为氧化反应,⑥为消去反应,
故答案为:②;
(3)反应②的化学方程式为:CH2BrCH2Br+2NaOH$\stackrel{△}{→}$HOCH2CH2OH+2NaBr;
反应⑦的化学方程式为:CaC2+2H2O=Ca(OH)2+C2H2↑,
故答案为:CH2BrCH2Br+2NaOH$\stackrel{△}{→}$HOCH2CH2OH+2NaBr;CaC2+2H2O=Ca(OH)2+C2H2↑;
Ⅱ.X与氯气在光照条件下得到一氯环己烷,故X为 ,一氯环己烷在氢氧化钠醇溶液、加热条件下发生消去反应生成
,一氯环己烷在氢氧化钠醇溶液、加热条件下发生消去反应生成 ,环己烯与溴发生加成反应生成Y为
,环己烯与溴发生加成反应生成Y为 ,在氢氧化钠醇溶液、加热条件下发生消去反应生成生成
,在氢氧化钠醇溶液、加热条件下发生消去反应生成生成
(4)反应①属于取代反应,反应②需要试剂:氢氧化钠的乙醇溶液、加热,属于消去反应,反应③需要试剂:溴的四氯化碳溶液或溴水,属于加成反应,
故答案为:
| ① | ② | ③ | |
| 试剂及条件 | ---- | 氢氧化钠的乙醇溶液、加热 | 溴的四氯化碳溶液或溴水 |
| 反应类型 | 取代反应 | 消去反应 | 加成反应 |
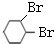
 +2NaOH $→_{△}^{醇}$
+2NaOH $→_{△}^{醇}$  +2NaBr+2H2O,
+2NaBr+2H2O, +2NaOH $→_{△}^{醇}$
+2NaOH $→_{△}^{醇}$  +2NaBr+2H2O;
+2NaBr+2H2O; 中碳碳双键断裂氧化生成-CHO,反应方程式为:
中碳碳双键断裂氧化生成-CHO,反应方程式为: $→_{(2)Zn,H_{2}O}^{(1)O_{3}}$OHC-CH2CH2CHO+OHC-CHO,产物中含氧官能团的名称是:醛基,
$→_{(2)Zn,H_{2}O}^{(1)O_{3}}$OHC-CH2CH2CHO+OHC-CHO,产物中含氧官能团的名称是:醛基,点评 本题考查有机物的推断,属于拼合型题目,涉及官能团的结构、有机反应类型、有机方程式书写、限制条件同分异构体书写等,注意根据有机物的结构与反应条件进行推断,需要学生熟练掌握官能团的性质与转化,难度中等.


 智慧课堂密卷100分单元过关检测系列答案
智慧课堂密卷100分单元过关检测系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 晶体熔点的高低: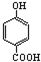 > >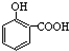 | |
| B. | 原子的价层电子数目的多少:Fe>As>K | |
| C. | 分子中的键角大小:CO2>H2O>NH3 | |
| D. | 微粒半径的大小:O2->F->Na+>Li+ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 选项 | A | B | C | D |
| n(CO2)(mol) | 2 | 3 | 4 | 6 |
| n(沉淀)(mol) | 1 | 2 | 3 | 2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
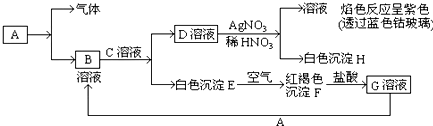
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸氢钠溶液中加入氢氧化钠溶液:H++OH-=H2O | |
| B. | 氧化铜和稀盐酸:CuO+2H+=Cu2++H2O | |
| C. | 少量的NaHCO3与足量的NaOH溶液:HCO3-+OH-=CO32-+H2O | |
| D. | 少量的NaHCO3溶液与足量的Ca(OH)2溶液:2HCO3-+Ca2++2OH-=CaCO3↓+CO32-+2H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com