
 =0.1mol,n(H)=2n(H2O)=2×0.1mol=0.2mol;
=0.1mol,n(H)=2n(H2O)=2×0.1mol=0.2mol; =0.05mol,n(C)=n(CO2)=0.05mol,某气态烃的物质的量为
=0.05mol,n(C)=n(CO2)=0.05mol,某气态烃的物质的量为 =0.05mol,
=0.05mol,

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:阅读理解
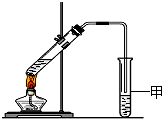 (1)甲物质只含有碳、氢两种元素,在标准状况下为气态,有机物甲的产量可以用来衡量一个国家的石油化工发展水平.工业上可以用丙物质来生产甲物质,反应式表示:
(1)甲物质只含有碳、氢两种元素,在标准状况下为气态,有机物甲的产量可以用来衡量一个国家的石油化工发展水平.工业上可以用丙物质来生产甲物质,反应式表示:| 500℃ |
| Cu或Ag |
| △ |
| Cu或Ag |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
A.H2+1/2O2![]() H2O ΔH=-12.76 kJ·mol-1??
H2O ΔH=-12.76 kJ·mol-1??
B.H2(g)+1/2O2(g) ![]() H2O(l) ΔH=-12.76 kJ·mol-1??
H2O(l) ΔH=-12.76 kJ·mol-1??
C.H2(g)+ 1/2O2(g)![]() H2O(l) ΔH=-285.8 kJ·mol-1??
H2O(l) ΔH=-285.8 kJ·mol-1??
D.2H2(g)+ O2(g)![]() 2H2O(l) ΔH=-571.6 kJ·mol-1?
2H2O(l) ΔH=-571.6 kJ·mol-1?
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)写出M的氢氧化物和碳酸氢钠反应的化学方程式________________________。
(2)要计算出M的相对原子质量,你认为还必须提供下列哪些数据____________________(填序号)。
A.M的氢氧化物溶液的物质的量浓度(设为2 mol·L-1)
B.M的碳酸盐沉淀的质量(设为39.4 g)
C.与M的碳酸盐反应的盐酸的物质的量浓度(设为0.1 mol·L-1)
D.题设条件充足,不需要补充数据
(3)根据你的选择,试计算金属M的相对原子质量和加入的NaHCO3溶液中溶质的质量。
查看答案和解析>>
科目:高中化学 来源:2011-2012年浙江省温州龙湾中学高一上学期第一次月考化学试卷 题型:单选题
下列判断中正确的是 ( )
| A.在标准状况下,1 mol水的体积约为22.4 L |
| B.在标准状况下,氧气的气体摩尔体积约为22.4 L |
| C.常温常压下,1 mol氢气的体积为22.4L |
| D.常温常压下,1 mol氧气的质量为32克 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com