
我国第五套人民币中的一元硬币材料为钢芯镀镍,依据你所掌握的电镀原理,你认为在硬币制作时,钢芯应做( )
A.阴极 B.阳极
C.正极 D .负极
.负极
科目:高中化学 来源: 题型:
已知蓄电池在充电时作电解池,放电时作原电池。铅蓄电池上有两个接线柱,一个接线柱旁标有“+”,另一个接线柱旁标有“-”。关于标有“+”的接线柱,下列说法中正确的是( )
A.充电时作阳极,放电时作正极
B.充电时发生还原反应,放电时发生氧化反应
C.充电时作阴极,放电时作负极
D.充电、放电时均发生氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示,在不同的电解质溶液中可以组 成不同的电池。
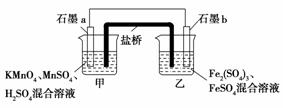
(1)①当电解质溶液为稀硫酸时,Fe电极是______(填“正”或“负”)极,其电极反应式为____________________________________________________________。
②当电解质溶液为NaOH溶液时,Al电极是______(填“正”或“负”)极,其电极反应式为________________________。
(2)若把铝改为锌,电解质溶液为浓硝酸,则Fe电极是______(填“正”或“负”)极,其电极反应式为________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
对金属制品进行抗腐蚀处理,可延长其使用寿命。
(1)以下为铝材表面处理的一种方法:
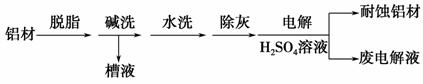
①碱洗的目的是除去铝材表面的自然氧化膜,碱洗时常有气泡冒出,原因是_________________________________
(用离子方程式表示)。为将碱洗槽液中的铝以沉淀形式回收,最好向槽液中加入下列试剂中的________。
a.NH3 b.CO2 c.NaOH d.HNO3
②以铝材为阳极,在H2SO4溶液中电解,铝材表面形成氧化膜,阳极电极反应式为_______________________________________________________。
取少量废电解液,加入NaHCO3溶液后产生气泡和白色沉淀,产生沉淀的原因是_________________________________________________________。
(2)镀铜可防止铁制品腐蚀,电镀时用铜而不用石墨作阳极的原因是_________________________________________________________________。
(3)利用右图装置,可以模拟铁的电化学防护。
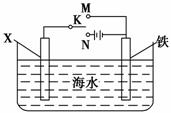
若X为碳棒,为减缓铁的腐蚀,开关K应置于________处。若X为锌,开关K置于M处,该电化学防护法称为______________________________ _____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学活动小组想通过如图所示装置(夹持装置已略去)进行实验,探究Na2O2与NO反应的产物。
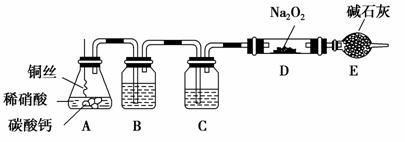
实验前,他们查阅有关资料得到如下信息:
①2NaNO3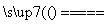 2NaNO2+O2↑;
2NaNO2+O2↑;
②NaNO2为白色粉末状固体,既有氧化性又有还原性;
③NaNO2溶液显弱碱性(原因:强碱弱酸盐的水解)。
实验开始时,先在A装置中加入适量的碳酸钙和足量稀硝酸,待不再有气体产生时,将铜丝插入稀硝酸中。
请回答下列问题:
(1)A装置中放入碳酸钙的目的是_____________________________________。
(2)装置B、C中的试剂分别是:B________、C________,E的作用是______________________________________________________________。
(3)如何检验反应中是否有氧气生成? _______________________________。
(4)假如Na2O2已反应完全,为确定D中固体产物的成分,甲同学将固体溶于水后,经测定发现溶液显强碱性,再向溶液中加入酸性高锰酸钾溶液,紫色退去。由此现象推断固体产物中可能含有的物质是________(填化学式)。
(5)乙同学取适量固体于试管中密闭加热,发现白色固体部分变为淡黄色。此现象说明固体中还可能含有的成分是________(填化学式)。根据以上推测,请写出Na2O2与NO反应的化学方程式_________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com