
| A. | 聚乙烯塑料的老化是由于发生了加成反应 | |
| B. | 乙酸乙酯在碱性条件下的水解反应称为皂化反应 | |
| C. | 葡萄糖注射液不能产生丁达尔效应现象,不属于胶体 | |
| D. | 棉、麻、合成纤维完全燃烧都只生成CO2和H2O |
分析 A.聚乙烯塑料的老化发生氧化反应;
B.油脂在碱性条件下水解为皂化反应;
C.葡萄糖注射液为溶液;
D.合成纤维是以小分子的有机化合物为原料,经加聚反应或缩聚反应合成的线型有机高分子化合物,分子中出C、H元素外,还含有其它元素,如N元素等.
解答 解:A.聚乙烯塑料的老化发生氧化反应,不含碳碳双键,不能发生加成反应,故A错误;
B.油脂为高级脂肪酸甘油酯,在碱性条件下水解为皂化反应,故B错误;
C.葡萄糖注射液为溶液,则不能产生丁达尔效应现象,不属于胶体,故C正确;
D.合成纤维是分子中出C、H元素外,还含有其它元素,如N元素等,燃烧还生成氮气等,而棉、麻完全燃烧都只生成CO2和H2O,故D错误;
故选C.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重分析与应用能力的考查,注意有机物的组成及有机反应,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 1molH2O2的质量为34g•mol-1 | |
| B. | C2H5OH的摩尔质量为46g | |
| C. | 3.01×1023个SO2分子的质量为32g | |
| D. | 1mol任何物质均含有6.02×1023个分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有③ | B. | 只有① | C. | ①和② | D. | 都正确 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
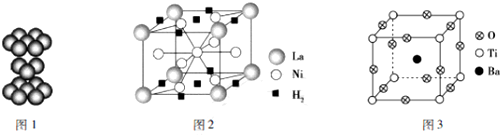
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
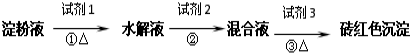
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
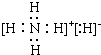 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
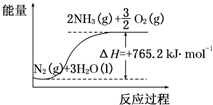 一种“人工固氮”的新方法是在常温、常压、光照条件下,N2在催化剂表面与水发生反应生成NH3:N2+3H2O?2NH3+$\frac{3}{2}$O2,进一步研究NH3生成量与温度的关系,部分实验数据见表(反应时间3h):
一种“人工固氮”的新方法是在常温、常压、光照条件下,N2在催化剂表面与水发生反应生成NH3:N2+3H2O?2NH3+$\frac{3}{2}$O2,进一步研究NH3生成量与温度的关系,部分实验数据见表(反应时间3h):| T/℃ | 30 | 40 | 50 |
| 生成NH3量/(10-6 mol) | 4.8 | 5.9 | 6.0 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com