
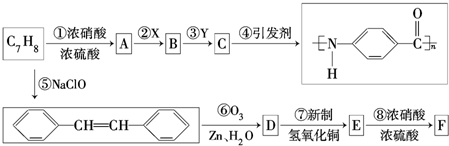
 .
. .
. $\stackrel{引发剂}{→}$
$\stackrel{引发剂}{→}$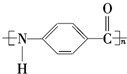 +n H2O、
+n H2O、 +2Cu(OH)2$\stackrel{△}{→}$Cu2O↓+2H2O+
+2Cu(OH)2$\stackrel{△}{→}$Cu2O↓+2H2O+ 、
、 +HNO3$→_{△}^{浓H_{2}SO_{4}}$
+HNO3$→_{△}^{浓H_{2}SO_{4}}$ +H2O.
+H2O. 分析 C7H8为 ,在浓硫酸作催化剂、加热条件下和浓硝酸发生取代反应生成A,A和X反应生成B,B和Y反应生成C,C发生反应生成某聚酰胺类物质(C7H5NO)n,根据某聚酰胺类物质(C7H5NO)n的结构简式知,反应④发生缩聚反应,则C的结构简式为:
,在浓硫酸作催化剂、加热条件下和浓硝酸发生取代反应生成A,A和X反应生成B,B和Y反应生成C,C发生反应生成某聚酰胺类物质(C7H5NO)n,根据某聚酰胺类物质(C7H5NO)n的结构简式知,反应④发生缩聚反应,则C的结构简式为: ,
, 和硝酸发生对位取代生成A是
和硝酸发生对位取代生成A是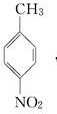 ,氨基易被氧化,所以A先发生氧化反应生成B是
,氨基易被氧化,所以A先发生氧化反应生成B是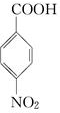 ,对硝基苯甲酸被还原生成C,根据信息②可知D为
,对硝基苯甲酸被还原生成C,根据信息②可知D为 ,与新制氢氧化铜反应生成E为
,与新制氢氧化铜反应生成E为 ,E与浓硝酸和浓硫酸间位取代生成F为
,E与浓硝酸和浓硫酸间位取代生成F为 .
.
解答 解:C7H8为 ,在浓硫酸作催化剂、加热条件下和浓硝酸发生取代反应生成A,A和X反应生成B,B和Y反应生成C,C发生反应生成某聚酰胺类物质(C7H5NO)n,根据某聚酰胺类物质(C7H5NO)n的结构简式知,反应④发生缩聚反应,则C的结构简式为:
,在浓硫酸作催化剂、加热条件下和浓硝酸发生取代反应生成A,A和X反应生成B,B和Y反应生成C,C发生反应生成某聚酰胺类物质(C7H5NO)n,根据某聚酰胺类物质(C7H5NO)n的结构简式知,反应④发生缩聚反应,则C的结构简式为: ,
, 和硝酸发生对位取代生成A是
和硝酸发生对位取代生成A是 ,氨基易被氧化,所以A先发生氧化反应生成B是
,氨基易被氧化,所以A先发生氧化反应生成B是 ,对硝基苯甲酸被还原生成C,根据信息②可知D为
,对硝基苯甲酸被还原生成C,根据信息②可知D为 ,与新制氢氧化铜反应生成E为
,与新制氢氧化铜反应生成E为 ,E与浓硝酸和浓硫酸间位取代生成F为
,E与浓硝酸和浓硫酸间位取代生成F为 .
.
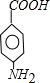
(1)氨基易被氧化,所以 先被酸性高锰酸钾溶液氧化生成
先被酸性高锰酸钾溶液氧化生成 ,再被Fe/HCl还原生成
,再被Fe/HCl还原生成 ,故答案为:B;
,故答案为:B;
(2)由上述分析可知,C的结构简式是 ,故答案为:
,故答案为: ;
;
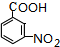
(3)物质F的结构简式为 ,故答案为:
,故答案为: ;
;
(4)对物质C( )的下列说法中,
)的下列说法中,
A.含有羧基,能发生酯化反应,故A正确;
B.不能与溴水发生加成反应,故B错误;
C.含有羧基与氨基,既能和碱反应又能和酸反应,故C错误,
故选:A;
(5)反应④的方程式为:n $\stackrel{引发剂}{→}$
$\stackrel{引发剂}{→}$ +n H2O,
+n H2O,
反应⑦的方程式为: +2Cu(OH)2$\stackrel{△}{→}$Cu2O↓+2H2O+
+2Cu(OH)2$\stackrel{△}{→}$Cu2O↓+2H2O+ ,
,
反应⑧的方程式为: +HNO3$→_{△}^{浓H_{2}SO_{4}}$
+HNO3$→_{△}^{浓H_{2}SO_{4}}$ +H2O,
+H2O,
故答案为:n $\stackrel{引发剂}{→}$
$\stackrel{引发剂}{→}$ +n H2O;
+n H2O; +2Cu(OH)2$\stackrel{△}{→}$Cu2O↓+2H2O+
+2Cu(OH)2$\stackrel{△}{→}$Cu2O↓+2H2O+ ;.
;. +HNO3$→_{△}^{浓H_{2}SO_{4}}$
+HNO3$→_{△}^{浓H_{2}SO_{4}}$ +H2O.
+H2O.
点评 本题主要考查有机推断,注意根据有机物的结构与给予的信息进行分析判断,熟练掌握官能团的性质与转化,有利于培养学生的逻辑推理能力、知识迁移运用能力.


科目:高中化学 来源: 题型:选择题
| A. | 中子数 | B. | 电子数 | C. | 原子序数 | D. | 质子数 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ③能与水在一定条件下反应生成C
③能与水在一定条件下反应生成C
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铅蓄电池属于二次电池 | |
| B. | 锂离子电池是一种一次性电池 | |
| C. | 氢氧燃料电池可把化学能转化为电能 | |
| D. | 镍镉电池中,Cd为负极,NiO(OH)为正极 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
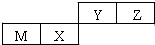
| A. | 原子半径Z>Y | |
| B. | Y的最高价氧化物对应水化物的酸性比X 的弱 | |
| C. | M和Y的最高价氧化物对应水化物之间能相互反应 | |
| D. | Y的气态氢化物比Z气态氢化物稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | ||
| Y | Z |
| A. | 化合物XZ3中各原子均满足8电子的稳定结构 | |
| B. | X、Y、Z三种元素形成的含氧酸都是强酸 | |
| C. | 常温下,Z单质可与Y的氢化物发生置换反应 | |
| D. | Z的气态氢化物比Y的气态氢化物更加稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
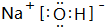 ,该化合物中所含的化学键有离子键、共价键.
,该化合物中所含的化学键有离子键、共价键.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com