
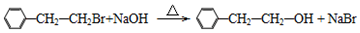 £®
£®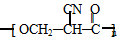 £ØŅŖÖŲŠĀŠ“¹ż£© µÄŗĻ³ÉĀ·ĻߣŗNCCH2CHO$”ś_{”÷}^{ŠĀÖĘCu£ØOH£©_{2}}$ $\stackrel{H+}{”ś}$
£ØŅŖÖŲŠĀŠ“¹ż£© µÄŗĻ³ÉĀ·ĻߣŗNCCH2CHO$”ś_{”÷}^{ŠĀÖĘCu£ØOH£©_{2}}$ $\stackrel{H+}{”ś}$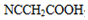 ”ś
”ś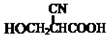 ”ś
”ś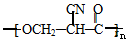 £®
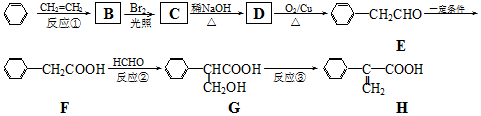
£® ·ÖĪö ±Č½Ļ±½ŗĶEµÄ½į¹¹¼ņŹ½æÉÖŖ£¬±½ÓėŅŅĻ©·¢Éś¼Ó³É·“Ӧɜ³ÉBĪŖC6H5-C2H5£¬BÓėäå·¢ÉśČ”“śÉś³ÉCĪŖC6H5-CH2CH2Br£¬C¼īŠŌĖ®½āµĆDĪŖC6H5-CH2CH2OH£¬DŃõ»ÆµĆE£¬EŃõ»ÆµĆF£¬FÓė¼×Č©·¢Éś¼Ó³ÉÉś³ÉG£¬G·¢ÉśĻūČ„·“Ó¦µĆH£¬ÓÉNCCH2CHOĪŖĘšŹ¼ŌĮĻÖʱø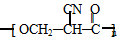 £¬æÉŅŌÓĆNCCH2CHOŃõ»ÆµĆNCCH2COOH£¬NCCH2COOHÓė¼×Č©·¢Éś¼Ó³É·“Ó¦µĆHOCH2CH£ØCN£©COOH£¬HOCH2CH£ØCN£©COOH·¢ÉśĖõ¾Ū·“Ó¦µĆ
£¬æÉŅŌÓĆNCCH2CHOŃõ»ÆµĆNCCH2COOH£¬NCCH2COOHÓė¼×Č©·¢Éś¼Ó³É·“Ó¦µĆHOCH2CH£ØCN£©COOH£¬HOCH2CH£ØCN£©COOH·¢ÉśĖõ¾Ū·“Ó¦µĆ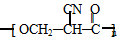 £¬¾Ż“Ė“šĢā£®
£¬¾Ż“Ė“šĢā£®
½ā“š ½ā£ŗ£Ø1£©øł¾ŻHµÄ½į¹¹¼ņŹ½æÉÖŖ£¬HÖŠµÄŗ¬Ńõ¹ŁÄÜĶÅĆū³ĘŹĒōČ»ł£¬
¹Ź“š°øĪŖ£ŗōČ»ł£»
£Ø2£©BĪŖC6H5-C2H5£¬BµÄĆū³ĘŹĒŅŅ±½£¬·Ö×ÓÖŠÓė±½»·ĻąĮ¬µÄĖłÓŠŌ×Ó¶¼¹²Ćę£¬ŅŅ»łÖŠ×ī¶ą3øöŌ×ÓŌŚ±½»·µÄĆęÉĻ£¬ĖłŅŌ¹²ÓŠ14øöŌ×Ó¹²Ćę£¬
¹Ź“š°øĪŖ£ŗŅŅ±½£»14£»
£Ø3£©øł¾ŻÉĻĆęµÄ·ÖĪöæÉÖŖ£¬·“Ó¦1µÄ·“Ó¦ĄąŠĶĪŖ¼Ó³É·“Ó¦£¬·“Ó¦2µÄ·“Ó¦ĄąŠĶĪŖ¼Ó³É·“Ó¦£¬
¹Ź“š°øĪŖ£ŗ¼Ó³É£»¼Ó³É£»
£Ø4£©C”śDµÄ»Æѧ·½³ĢŹ½ĪŖ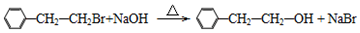 £¬
£¬
¹Ź“š°øĪŖ£ŗ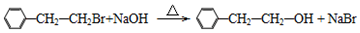 £»
£»
£Ø5£©øł¾ŻĢõ¼ž¢ŁÄÜ·¢ÉśŅų¾µ·“Ó¦ŗĶĖ®½ā·“Ó¦£¬ĖµĆ÷ÓŠ¼×Ėįijõ„£¬¢ŚÄÜÓėFeCl3·¢ÉśĻŌÉ«·“Ó¦£¬ĖµĆ÷ÓŠ·ÓōĒ»ł£¬¢Ū±½»·ÉĻŗ¬ÓŠ3øö²»ĻąĶ¬µÄČ”“ś»ł£¬ŌņĀś×ćĻĀĮŠĢõ¼žµÄGµÄĶ¬·ÖŅģ¹¹ĢåĪŖ±½»·ÉĻĮ¬ÓŠ-OOCH”¢-OH”¢-CH2CH3£¬»ņ-CH2OOCH”¢-OH”¢-CH3£¬ĆæŅ»ÖÖĒéæö¶¼æÉŅŌøł¾Ż¶Ø¶ž¶ÆŅ»µÄŌŌņæÉÖŖ£¬ĆæÖÖĒéæö¶¼ÓŠ10ÖÖ½į¹¹£¬Ōņ·ūŗĻĢõ¼žµÄGµÄĶ¬·ÖŅģ¹¹ĢåÓŠ20ÖÖ£¬
¹Ź“š°øĪŖ£ŗ20£»
£Ø6£©ÓÉNCCH2CHOĪŖĘšŹ¼ŌĮĻÖʱø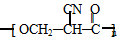 £¬ÓĆNCCH2CHOŃõ»ÆµĆNCCH2COOH£¬NCCH2COOHÓė¼×Č©·¢Éś¼Ó³É·“Ó¦µĆHOCH2CH£ØCN£©COOH£¬HOCH2CH£ØCN£©COOH·¢ÉśĖõ¾Ū·“Ó¦µĆ
£¬ÓĆNCCH2CHOŃõ»ÆµĆNCCH2COOH£¬NCCH2COOHÓė¼×Č©·¢Éś¼Ó³É·“Ó¦µĆHOCH2CH£ØCN£©COOH£¬HOCH2CH£ØCN£©COOH·¢ÉśĖõ¾Ū·“Ó¦µĆ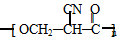 £¬ŗĻ³ÉĀ·ĻßĪŖ
£¬ŗĻ³ÉĀ·ĻßĪŖ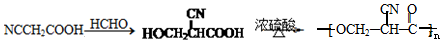 £¬
£¬
¹Ź“š°øĪŖ£ŗ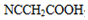 ”¢
Ӣ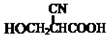 Ӣ
”¢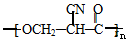 £®
£®
µćĘĄ ±¾ĢāÉę¼°ÓŠ»ś»ÆŗĻĪļÖ®¼äµÄ×Ŗ»Æ¹ŲĻµ”¢¹ŁÄÜĶż°ŠŌÖŹ”¢ÓŠ»ś·“Ó¦ĄąŠĶ”¢ÓŠĢõ¼žµÄĶ¬·ÖŅģ¹¹ĢåµÄŹéŠ“”¢ÓŠ»śŗĻ³ÉµČĻą¹ŲÖŖŹ¶£¬Ć÷Č·ÓŠ»śĪļµÄ¹ŁÄÜĶż°ĘäŠŌÖŹŹĒ½ā±¾Ģā¹Ų¼ü£¬ÄѶČÖŠµČ£®


 æĘѧŹµŃé»ī¶Æ²įĻµĮŠ“š°ø
æĘѧŹµŃé»ī¶Æ²įĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | ŌŚĻąĶ¬Ģõ¼žĻĀ£¬pH=5µÄCH3COOHČÜŅŗŗĶpH=5µÄNH4ClČÜŅŗÖŠ£¬Ė®µÄµēĄė³Ģ¶Č²»ĻąĶ¬ | |
| B£® | ·“Ó¦NH3£Øg£©+HCl£Øg£©?NH4Cl£Øs£©ÄÜ×Ō·¢½ųŠŠ£¬ŌņøĆ·“Ó¦”÷H£¼0 | |
| C£® | ŠæÓėĻ”ĮņĖį·“Ó¦Ź±¼ÓČėÉŁĮæĮņĖįĶ£¬·“Ó¦¼ÓæģµÄÖ÷ŅŖŌŅņŹĒCu2+Ė®½āŌö“óĮĖ c£ØH+£© | |
| D£® | Ņ»¶ØĢõ¼žĻĀ£¬·“Ó¦2SO2£Øg£©+O2£Øg£©?2SO3£Øg£©”÷H£¼0“ļµ½Ę½ŗāŗó£¬ÉżøßĢåĻµĪĀ¶Č£¬Ó¦ÖŲŠĀ“ļµ½Ę½ŗāĒ°£¬ÓŠvÕż£ØO2£©£¾2vÄę£ØSO2£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1.204”Į1024øö | B£® | 6.02”Į1023øö | C£® | 4.816”Į1023øö | D£® | 2.408”Į1023øö |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¹¤ŅµÉĻæÉÓĆĀĮČČ·“Ó¦“ó¹ęÄ£Į¶Ģś | B£® | SO2³£ÓĆÓŚÖ½ÕŵČÖ²ĪļĻĖĪ¬µÄĘÆ°× | ||
| C£® | SiŹĒÖŲŅŖµÄ°ėµ¼Ģå²ÄĮĻ | D£® | µē½āČŪČŚMgCl2£¬æÉÖĘµĆ½šŹōĆ¾ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ·Ö×Ó×ÜŹżĪŖNAµÄNO2ŗĶCO2»ģŗĻĘųĢåÖŠŗ¬ÓŠµÄŃõŌ×ÓŹżĪŖ2NA | |
| B£® | 0.5 mol O3Óė11.2 L O2Ėłŗ¬µÄ·Ö×ÓŹżŅ»¶ØĻąµČ | |
| C£® | ĪļÖŹµÄĮæÅضČĪŖ0.5 mol/L MgCl2ČÜŅŗ£¬ŗ¬ÓŠCl-ŹżĪŖNA | |
| D£® | ±źæöĻĀ£¬22.4 LĖÄĀČ»ÆĢ¼µÄÖŹĮæĪŖ154 g |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ČŻĘ÷ | ¼× | ŅŅ |
| ·“Ó¦ĪļĶ¶ČėĮæ | 1mol CO2£Øg£©ŗĶ3mol H2£Øg£© | 1mol CH3OH £Øg£©ŗĶ 1mol H2O£Øg£© |
| Ę½ŗāŹ±c£ØCH3OH£© | c1 | c2 |
| Ę½ŗāŹ±ÄÜĮæ±ä»Æ | ·Å³ö29.4kJ | ĪüŹÕa kJ |
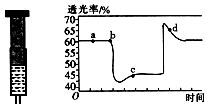
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ü£¾¢Ś£¾¢Ū£¾¢Ł | B£® | ¢Ł£¾¢Ü£¾¢Ś£¾¢Ū | C£® | ¢Ł£¾¢Ś£¾¢Ū£¾¢Ü | D£® | ¢Ü£¾¢Ł£¾¢Ū£¾¢Ś |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | KClµÄĦ¶ūÖŹĮæŹĒ£ŗ74.5g | B£® | Ņ»Ė®ŗĻ°±µÄ»ÆѧŹ½ĪŖ£ŗNH4•OH | ||
| C£® | Na2O2ÖŠµÄŅõĄė×ÓĪŖ£ŗO2- | D£® | Ć¾µÄŌ×Ó½į¹¹Ź¾ŅāĶ¼ČēĶ¼ĖłŹ¾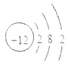 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com