
【题目】A、B、C、D四种短周期元素,原子序数D>A>B>C,且A、B同周期,C、D同主族,A的原子结构示意图如图,B元素最外层电子数是次外层电子数的四分之一,C元素的气态氢化物的水溶液显碱性,据此填空:

(1)A元素气态氢化物的电子式___,A、B、C、D四种元素按原子半径由大到小的顺序排列为___。(填元素符号)
(2)A的最高价氧化物与氢氧化钠反应的离子方程式为___。
(3)A,C,D的最高价氧化物对应水化物的酸性强弱_______,C的氢化物比D的氢化物沸点___(填“高”或“低”),原因是___。
【答案】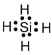 Mg>Si>P>N SiO2+2OH-=SiO32-+H2O HNO3>H2SiO3>H3PO4 高 NH3分子之间存在氢键
Mg>Si>P>N SiO2+2OH-=SiO32-+H2O HNO3>H2SiO3>H3PO4 高 NH3分子之间存在氢键
【解析】
A、B、C、D四种短周期元素,原子序数D>A>B>C,根据A的原子结构示意图可知,x=2,A的质子数为14,则A为Si元素,B元素最外层电子数是次外层电子数的四分之一,B元素原子有3个电子层,最外层电子数为2,所以B为Mg元素,C元素的气态氢化物的水溶液显碱性,则C为N元素,C、D同主族,则D为P元素,根据元素所在周期中的位置结合周期律的递变规律解答此题。
A、B、C、D四种短周期元素,原子序数D>A>B>C,根据A的原子结构示意图可知,x=2,A的质子数为14,则A为Si元素,B元素最外层电子数是次外层电子数的四分之一,B元素原子有3个电子层,最外层电子数为2,所以B为Mg元素,C元素的气态氢化物的水溶液显碱性,则C为N元素,C、D同主族,则D为P元素。
(1)由以上分析可知A为Si元素,其气态氢化物为SiH4,分子中氢原子与硅原子之间形成1对共用电子对,电子式为: ;同周期自左而右原子半径减小,同主族自上而下原子半径增大,所以A、B、C、D四种元素按原子半径由大到小的顺序排列为:Mg>Si>P>N;
;同周期自左而右原子半径减小,同主族自上而下原子半径增大,所以A、B、C、D四种元素按原子半径由大到小的顺序排列为:Mg>Si>P>N;
(2)A的最高价氧化物为SiO2,与氢氧化钠反应的离子方程式为:SiO2+2OH-=SiO32-+H2O;
(3)元素的非金属性越强,对应最高价氧化物对应水化物的酸性越强,非金属性:N>P>Si,则酸性:HNO3> H3PO4 > H2SiO3,NH3分子之间存在氢键,所以其沸点比PH3的沸点高。


科目:高中化学 来源: 题型:
【题目】中学化学中几种常见物质的转化关系如下图所示:
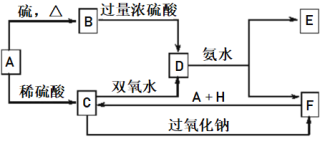
已知A是一种单质,将D溶液滴入沸水中可得到以F为分散质的红褐色胶体。请回答下列问题:
(1)写出C的溶液与双氧水反应的离子方程式:_________________。
(2)写出鉴定E中阳离子的实验方法和现象:________________。
(3)F是一种难溶物质,其溶度积常数为1.0×10-39。向D溶液中加碱调节至pH为_______时,铁离子刚好沉淀完全(离子浓度小于1.0×10-5 mol·L-1时,即可认为该离子沉淀完全)。
(4)已知1mol SO2(g)氧化为1mol SO3(g)的ΔH= –99 kJ·mol-1,单质硫的燃烧热为296 kJ·mol-1,计算由S(s)生成3 molSO3(g)的△H=__________kJ·mol-1。
(5)在200 mL 1.5 mol·L-1 NaOH溶液中通入标准状况下4.48L CO2气体,完全反应后所得溶液中,各种离子浓度由大到小的顺序是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积一定的密闭容器中,进行可逆反应A(g)+2B(g) ![]() C(g) +D(g),有图Ⅰ、Ⅱ所示的反应曲线,下列说法中不正确的是( )
C(g) +D(g),有图Ⅰ、Ⅱ所示的反应曲线,下列说法中不正确的是( )

A. 正反应是放热反应
B. P1 <P2
C. 若P3<P4,y轴表示A的转化率
D. 若P3>P4,y轴表示C的体积分数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)用电子式表示H2O和MgBr2的形成过程:___、___。
(2)H2O以___键结合,MgBr2以___键结合。(填极性键、非极性键、离子键)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列有关图象,说法正确的是
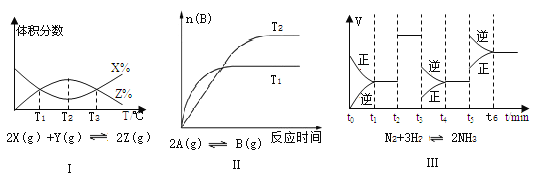
A. 由图Ⅰ知,该反应的△H>0 B. 由图Ⅱ知,该反应为放热反应
C. 由图Ⅲ知,t3时一定是采取降低反应温度的措施 D. 由图Ⅲ知,反应在t6时,NH3体积分数最大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:AgBr比AgCl更难溶,将AgCl与AgBr的饱和溶液等体积混合,再加入足量的浓AgNO3溶液,发生的反应为
A. 只有AgBr沉淀生成 B. AgCl与AgBr沉淀等量生成
C. AgCl与AgBr沉淀都有,但以AgCl沉淀为主 D. AgCl与AgBr沉淀都有,但以AgBr沉淀为主
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学一选修5:有机化学基础](15分)聚戊二酸丙二醇酯(PPG)是一种可降解的聚酯类高分子材料,在材枓的生物相容性方面有很好的应用前景。 PPG的一种合成路线如下:

已知:
①烃A的相对分子质量为70,核磁共振氢谱显示只有一种化学环境的氢;
②化合物B为单氯代烃:化合物C的分子式为C5H8;
③E、F为相对分子质量差14的同系物,F是福尔马林的溶质;
④![]() 。
。
回答下列问题:
(1)A的结构简式为 。
(2)由B生成C的化学方程式为 。
(3)由E和F生成G的反应类型为 ,G的化学名称为 。
(4)①由D和H生成PPG的化学方程式为 。
②若PPG平均相对分子质量为10000,则其平均聚合度约为 (填标号)。
a.48 b.58 c.76 d.122
(5)D的同分异构体中能同时满足下列条件的共有 种(不含立体异构):
①能与饱和NaHCO3溶液反应产生气体
②既能发生银镜反应,又能发生皂化反应
其中核磁共振氢谱显示为3组峰,且峰面积比为6:1:1的是 (写结构简式):
D的所有同分异构体在下列—种表征仪器中显示的信号(或数据)完全相同,该仪器是_____(填标号)。
a.质谱仪 b.红外光谱仪 c.元素分析仪 d.核磁共振仪
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作对应的现象符合事实的是( )
|
|
|
|
A.将绿豆大小的金属钠投入蒸馏水中,钠块熔成小球,浮于水面,迅速游 动,溶液变红 | B.将甲烷与氯气1∶1混合,在光照条件下反应,黄绿色褪去,水面上升,充满集气瓶 | C.将5g碳酸钙投入20mL1mol·L-1盐酸,针筒活塞向右移动的速率先逐渐增大,然后减小 | D.将铜片与浓硫酸混合加热,品红溶液变红,试管内出现蓝色固体和 少量黑色物质 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验装置图的叙述中,正确的是

① ②
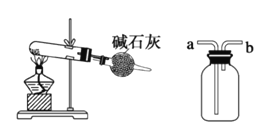
③ ④
A. 装置①:常用于分离互不相溶的液体混合物
B. 装置②:可用于吸收氯化氢、氨气等气体尾气,防止倒吸
C. 装置③:可用于实验室以氯化铵为原料制备少量NH3的实验
D. 装置④:先装满水,再从b口进NO气体,可收集NO
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com