
| A�� | ʵ�����С�ͨ��������ų��к������壬�ܷ�ֹ�к�������Ⱦ�������� | |
| B�� | ����̼�⻯�������������ŷſ�����Ч�ķ�ֹ�⻯ѧ�����IJ��� | |
| C�� | ��������������Ʒ��Ϊ�����ķ������û�ѧ�������������ϼӹ��ɷ�ˮͿ�ϻ����� | |
| D�� | �Է�����ؽ��м��л��պ�������ҪĿ���Ƿ�ֹ�ؽ����ӵ���Ⱦ |
���� A��ʵ�����С�ͨ������ǽ��к������ŷŵĴ����У�
B��̼�⻯�����������ɵ��¹⻯ѧ������
C��������������ɰ�ɫ��Ⱦ��
D������к��еĹ���ͭ���ؽ�����������ˮԴ������Ⱦ�ԣ�
��� �⣺A��ʵ�����С�ͨ������ǽ��к������ŷŵĴ����У�����ɿ�����Ⱦ����A����
B��̼�⻯�����������ɵ��¹⻯ѧ�������������к��������ŷſ�����Ч�ķ�ֹ�⻯ѧ�����IJ�������B��ȷ��
C��������������Ʒ�û�ѧ�����ӹ��ɷ�ˮͿ�ϻ����ͣ��ܼ��ٰ�ɫ��Ⱦ����C��ȷ��
D���Է�����ؽ��м��л��պ�������ҪĿ���Ƿ�ֹ�ؽ����ӵ���Ⱦ����D��ȷ��
��ѡ��A��
���� ���⿼�黯ѧ�������еĻ�����Ⱦ����������Ϥ���֪ʶ�ǽ���ؼ�����Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ������ | ȼ���� | ������ | ȼ���� |
| ���� | 891.0 | ������ | 2878.0 |
| ���� | 1560.8 | �춡�� | 2869.6 |
| ���� | 2221.5 | 2-������ | 3531.3 |
| A�� | ���ȶ��ԣ������飼�춡�� | |
| B�� | ����ȼ�յ��Ȼ�ѧ����ʽΪ�� 2C2H6��g��+7O2��g����4CO2��g��+6H2O��g����H=-1560.8KJ/mol | |
| C�� | �������ȼ���Ȳ�����3530 KJ/mol | |
| D�� | ��ͬ������������̼����������Խ����ȫȼ�շų�������Խ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
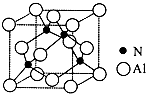 �� ��֪�������ľ����ṹ��ͼ��ʾ����ش��������⣮
�� ��֪�������ľ����ṹ��ͼ��ʾ����ش��������⣮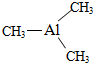 ������
�������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���Ӱ뾶��S2-��O2-��Na+��Al3+ | B�� | ���ȶ��ԣ�HCl��H2S��PH3��AsH3 | ||
| C�� | �縺�ԣ�F��O��N��C | D�� | ��һ�����ܣ�F��O��N��C |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ѧ�������Ĺ�ϵ��b��c | |
| B�� | �������ݻ���С�÷�Ӧ���淴Ӧ���ʼ�С | |
| C�� | ԭ��������BŨ�ȱ仯��ʾ�÷�Ӧ��1 min�ڵ�����Ϊ$\frac{cx}{b}$mol•��L•min��-1 | |
| D�� | �������¶Ⱥ������ݻ����䣬���뺤���������뷴Ӧ����ƽ�ⲻ�����ƶ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
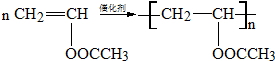 ��
��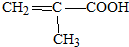 ��
��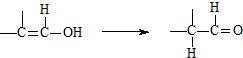
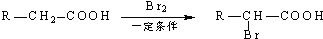
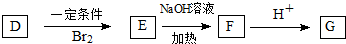
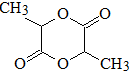 ��д��N������ȥ��Ӧ�Ļ�ѧ����ʽ��CH3CH��OH��COOH$��_{��}^{Ũ����}$CH2=CHCOOH+H2O��
��д��N������ȥ��Ӧ�Ļ�ѧ����ʽ��CH3CH��OH��COOH$��_{��}^{Ũ����}$CH2=CHCOOH+H2O���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
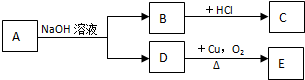
| A�� | 2�� | B�� | 3�� | C�� | 4�� | D�� | 5�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
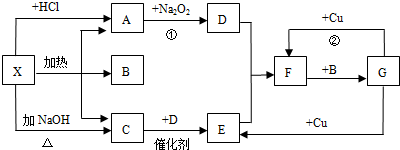
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 3.0g | B�� | 3.5g | C�� | 5.5g | D�� | 5.6g |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com