
Ag2Se单晶呈六角微型管状,有望开发为新型材料,其制取原理为4AgCl+3Se+6NaOH=2Ag2Se+Na2SeO3+4NaCl+3H2O。关于该反应的下列叙述正确的是( )
A.AgCl作氧化剂
B.6 mol NaOH参加反应转移6 mol e-
C.被还原的硒与被氧化的硒的质量之比为1∶2
D.被还原的硒与被氧化的硒的物质的量之比为2∶1
 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:高中化学 来源:2016-2017学年山西省高一上10月月考化学试卷(解析版) 题型:实验题
现用98%的浓H2SO4(ρ="1.84" g/cm3)配制成浓度为1.0mol/L的稀硫酸250 mL。
(1)现有主要仪器:A量筒 B烧杯 C玻璃棒 D胶头滴管 还缺少的仪器_______________;
(2)请将下列操作序号按正确顺序填在横线上:
A.用量筒量取浓H2SO4
B.反复颠倒摇匀
C.用胶头滴管加水至刻度
D.洗涤烧杯、玻璃棒2-3次
E.稀释浓H2SO4
F.冷却后将溶液转入容量瓶
其操作正确顺序为__________________;
(3)下列操作中,容量瓶所不具备的功能有________(填序号);
A.配制一定体积准确浓度的标准溶液
B.量取一定体积的液体
C.测量容量瓶规格以下的任意体积的液体
D.贮存溶液
E.用来加热和溶解固体溶质
(4)简要回答下列问题
①所需浓H2SO4的体积为___________mL;
②将浓H2SO4沿烧杯内壁慢慢注入盛水的烧杯中,不断搅拌,若搅拌过程中有液体溅出,会使最终结果_________ (填“偏高”、“偏低”或“无影响”,下同);若将量筒洗涤转移到容量瓶会使最终结果_________ ;定容时水加多后用滴管吸出会使结果_________;
(5)该浓硫酸与等质量的水混合所得溶液的物质的量浓度________9.2 mol/L (填“>”、“=”或“<”)。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江哈尔滨师大附中高二上期中化学卷(解析版) 题型:选择题
在空气中直接蒸发下列盐的溶液:①Fe2(SO4)3 ②Na2CO3 ③KCl ④CuCl2 ⑤NaHCO3可以得到相应盐的晶体(可以含有结晶水)的是
A.①③⑤ B.①②③ C.②④ D.①③④⑤
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江哈尔滨六中高一上期中化学试卷(解析版) 题型:选择题
在一定条件下,RO 和F2可发生如下反应:RO
和F2可发生如下反应:RO +F2+2OH-=RO
+F2+2OH-=RO +2F-+H2O,从而可知在RO
+2F-+H2O,从而可知在RO 中,元素R的化合价是( )
中,元素R的化合价是( )
A.+4价 B.+5价 C.+6价 D.+7价
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江哈尔滨六中高一上期中化学试卷(解析版) 题型:选择题
在T ℃时,将a g NH3完全溶于水,得到V mL溶液,假设该溶液的密度为ρ g·cm-3,溶质的质量分数为w,其中含NH4+的物质的量为b mol。下列叙述中正确的是( )
A.溶质的质量分数为w= ×100%
×100%
B.溶质的物质的量浓度c= mol·L-1
mol·L-1
C.溶液中c(OH-)= mol·L-1
mol·L-1
D.上述溶液中再加入V mL水后,所得溶液溶质的质量分数大于0.5w
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江哈尔滨六中高一上期中化学试卷(解析版) 题型:选择题
下列实验中,所采取的分离方法与对应原理都正确的是( )
选项 | 目的 | 分离方法 | 原理 |
A | 分离溶于水中的碘 | 乙醇萃取 | 碘在乙醇中的溶解度较大 |
B | 分离乙酸乙酯和乙醇 | 分液 | 乙酸乙酯和乙醇的密度不同 |
C | 除去KNO3固体中混杂的NaCl | 重结晶 | NaCl在水中的溶解度很大 |
D | 除去丁醇中的乙醚 | 蒸馏 | 丁醇与乙醚的沸点相差较大 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江哈尔滨六中高二上期中化学试卷(解析版) 题型:简答题
A、B、C、D、E五种物分别是NaOH、NH3·H2O、CH3COOH、HCl、NH4HSO4中的一种。常温下进行下列实验:
①0.001 mol/L的A溶液pH=3;
②B溶液和D溶液显碱性,等浓度两者PH关系B< D;
③E是弱电解质。回答下列问题:
(1)D是____________溶液,判断理由是______________________。
(2)用水稀释0.1 mol·L-1 B时,溶液中随着水量的增加而减小的是________(填写序号)。
①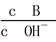 ②
②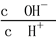 ③c(H+)和c(OH-)的乘积 ④OH-的物质的量
③c(H+)和c(OH-)的乘积 ④OH-的物质的量
(3)将等体积、等物质的量浓度B和C的溶液混合,升高温度(溶质不会分解)溶液pH随温度变化为图中的________曲线(填写序号)。
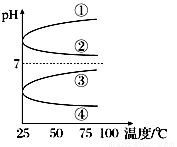
(4)OH-浓度相同的等体积的两份溶液A和E,分别与锌粉反应,若最后仅有一份溶液中存在锌,放出氢气的质量相同,则下列说法正确的是________(填写序号)。
①反应所需要的时间E>A ②开始反应时的速率A>E
③参加反应的锌的物质的量A=E ④反应过程的平均速率E>A
⑤A溶液里有锌剩余 ⑥E溶液里有锌剩余
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江哈尔滨六中高二上期中化学试卷(解析版) 题型:选择题
下列关于电解质电离的叙述中,正确的是
A.碳酸钙在水中溶解度很小,其溶液的电阻率很大,所以碳酸钙是弱电解质
B.碳酸钙在水中的溶解度很小,但被溶解的碳酸钙全部电离,所以碳酸钙是强电解质
C.氯气和氨气的水溶液导电性都很好,所以它们是强电解质
D.水难电离,纯水 几乎不导电,所以水是非电解质
几乎不导电,所以水是非电解质
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江大庆中学高二上期中化学试卷(解析版) 题型:选择题
在密闭体积不变的真空容器中加入一定量纯净的氨基甲酸铵固体(固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s) 2NH3(g)+CO2(g),已知25℃时,平衡气体总浓度为2.4×10-3mol·L-1,下列说法中正确的是( )
2NH3(g)+CO2(g),已知25℃时,平衡气体总浓度为2.4×10-3mol·L-1,下列说法中正确的是( )
A.密闭容器中气体的平均相对分子质量不变则该反应达到平衡状态
B.20℃时氨基甲酸铵的分解平衡常数为2.048×10-9mol3·L-3
C.恒温下压缩体积,NH3的体积分数不变
D.再加入一定量氨基 甲酸铵,可加快正反应反应速率
甲酸铵,可加快正反应反应速率
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com