
【题目】下列物质中可以用作净水剂的是
A. NaCl B. MgCl2 C. CuCl2 D. FeCl3
科目:高中化学 来源: 题型:
【题目】我国规定饮用水质量标准必须符合下列要求:
pH | 6.5~8.5 |
Ca2+、Mg2+总浓度 | <0.0045 mol·L-1 |
细菌总数 | <100个·mL-1 |
以下是源水处理成自来水的工艺流程示意图: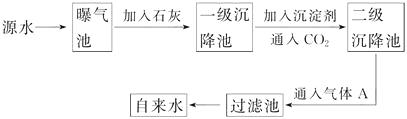
(1)源水中含Ca2+、Mg2+、HCO、Cl-等,加入石灰后有Ca(OH)2生成,进而发生若干复分解反应,写出其中一个离子方程式?
(2)凝聚剂除去悬浮固体颗粒的过程(填写编号)。
①只是物理过程 ②只是化学过程 ③是物理和化学过程
FeSO4·7H2O是常用的凝聚剂,它在水中最终生成沉淀。
(3)通入CO2的目的是。
(4)气体A的作用是 , 这种作用是基于气体A和水反应的产物具有性。
(5)下列物质中,可以作为气体A的代用品(填写编号)。
①Ca(ClO)2 ②NH3(液) ③K2FeO4 ④SO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有FeCl3、AlCl3的混合溶液100mL,逐滴加入NaOH溶液,生成沉淀的物质的量随加入的NaOH的物质的量的关系如图. 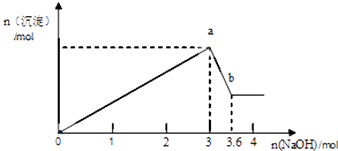
(1)a点对应的沉淀为(填化学式).
(2)计算原混合液中FeCl3的物质的量浓度为多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验中,所选装置不合理的是( ) 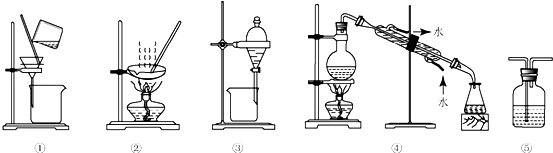
A.分离Na2CO3溶液和CCl4 , 选④
B.用CC14提取碘水中的碘,选③
C.用FeC12溶液吸收C12 , 选⑤
D.粗盐提纯,选①和②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏伽德罗常数的值,下列说法正确的是( )
A.100 g质量分数为98%的浓硫酸中所含有的氧原子数为4 NA
B.足量的Fe与6.72 L Cl2反应转移的电子数为0.6 NA
C.密闭容器中1 molN2与4 molH2反应生成的NH3分子数小于2NA
D.常温常压下,92 g的NO2和N2O4混合气体含有的氧原子数为3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,A处通入干燥Cl2 , 关闭B阀时,C处的红色布条看不到明显现象,打开B阀后,C处红色布条逐渐褪色,则D瓶中装的是( ) 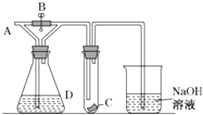
A.浓H2SO4
B.NaOH溶液
C.浓盐酸
D.饱和NaCl溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.石油分馏可以获得乙烯
B.煤经过气化和液化等物理变化可转化为淸洁燃料
C.聚乙烯塑料制品可用于食品包装
D.天然气和液化气的主要成分都是甲烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制取少量干燥的氨气涉及下列装置,其中正确的是( ) 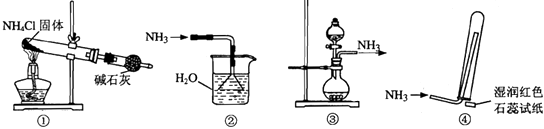
A.①是氨气发生装置
B.③是氨气发生装置
C.②是氨气吸收装置
D.④是氨气收集、检验装置
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为解决大气中CO2的含量增大的问题,某科学家提出“绿色自由”构想:把工厂排出的富含CO2的废气经净化吹入碳酸钾溶液吸收,然后再把CO2从溶液中提取出来,经化学反应使废气中的CO2转变为燃料甲醇.“绿色自由”构想的部分技术流程如图1 
(1)合成塔中反应的化学方程式为;△H<0.从平衡移动原理分析,低温有利于提高原料气的平衡转化率.而实际生产中采用300℃的温度,除考虑温度对反应速率的影响外,还主要考虑了 .
(2)从合成塔分离出甲醇的原理与下列操作的原理比较相符(填字母)
A.过滤
B.分液
C.蒸馏
D.结晶
(3)在体积为2L的合成塔中,充人2mol CO2和6mol H2 , 测得CO2(g)和CH3OH(g)的浓度随时间变化如图2所示. 从反应开始到平衡,V(H2)=;能使平衡体系中 ![]() 增大的措施有 .
增大的措施有 .
(4)如将CO2与H2以1:4的体积比混合,在适当的条件下可制得CH4 . 巳知
CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H1=﹣890.3kJ/mol
H2(g)+ ![]() O2(g)═H2O(l)△H2=﹣285.5kJ/mol
O2(g)═H2O(l)△H2=﹣285.5kJ/mol
写出CO2(g)与H2(g)反应生成CH4(g)与液态水的热化学方程式 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com