
分析 A、干冰是分子晶体,晶体中只含共价键,熔化时需要破坏分子间作用力;
B、铜是金属晶体,具有导电、导热、延展性,熔化时破坏金属键;
C、二氧化硅是原子晶体,熔化时需要破坏共价键;
D、氢氧化钠是离子晶体,晶体中既有离子键又有共价键,熔化时破坏离子键,由此分析解答.
解答 解:A、干冰是分子晶体,晶体中只含共价键,熔化时需要破坏分子间作用力;
B、铜是金属晶体,具有导电、导热、延展性,熔化时破坏金属键;
C、二氧化硅是原子晶体,熔化时需要破坏共价键;
D、氢氧化钠是离子晶体,晶体中既有离子键又有共价键,熔化时破坏离子键;
(1)晶体中存在分子的是干冰,故答案为:A;
(2)晶体中既有离子键又有共价键的是氢氧化钠,故答案为:D;
(3)熔化时需要破坏共价键的是二氧化硅,故答案为:C;
(4)具有导电、导热、延展性的是铜,故答案为:B.
点评 本题考查金属的通性,原子晶体的构成,离子晶体的性质,题目比较简单.


科目:高中化学 来源:2016-2017学年陕西省高二上月考一化学卷(解析版)) 题型:实验题
A.移取20.00mL待测的盐酸溶液注入洁净的锥形瓶,并加入2-3滴酚酞 |
B.用标准溶液润洗滴定管2-3次 |
C.把盛有标准溶液的碱式滴定管固定好,调节液面使滴定管尖嘴充满溶液 |
D.取标准KOH溶液注入碱式滴定管至0刻度以上2-3cm |
E.调节液面至0或0刻度以下,记下读数
F.把锥形瓶放在滴定管的下面,用标准KOH溶液滴定至终点,记下滴定管液面的刻度
完成以下填空:
(1)正确操作的顺序是(用序号字母填写)B-
(2)滴定开始后,眼睛注视 ,判断到达终点的现象是 。
(3)下列操作中可能使所测盐酸的浓度数值偏高的是
A 碱式滴定管未用标准溶液润洗就直接注入标准液
B 滴定前盛放HCl的锥形瓶用蒸馏水洗净后有少量水残留
C 碱式滴定管在滴定前有气泡,滴定后气泡消失
D 读取氢氧化钠溶液时,开始仰视读数,滴定结束时俯视读数
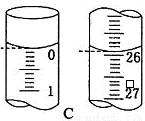
(4)滴定开始和结束时,碱式滴定管中的液面如图C所示,则终点读数为 mL,所测盐酸溶液的浓度为 mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 能使溴水褪色 | B. | 能与新制Cu(OH)2悬浊液反应 | ||
| C. | 与足量的氢气反应生成1-丙醇 | D. | 不能发生银镜反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 对于反应CH2=CH2(g)+H2(g)→CH3CH3(g)△H<0,若使用催化剂,反应过程中放出的热量更多 | |
| B. | CO燃烧的热化学方程式为2CO(g)+O2(g)=2CO2(g)△H=+285.8kJ/mol | |
| C. | 反应2Mg+CO2=2MgO+C△H<0从熵变角度看,不可自发进行 | |
| D. | 在密闭容器中,2HI(g)?H2(g)+I2(g)△H=+14.9kJ/mol,若投入NA个HI分子,反应平衡时,吸热7.45kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
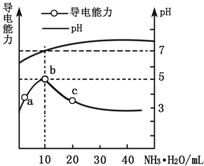 常温下,向10mL 0.1mol•L-1的HR溶液中逐滴滴入0.1mol•L-1的氨水,所得溶液pH及导电性变化如图.下列分析不正确的是( )
常温下,向10mL 0.1mol•L-1的HR溶液中逐滴滴入0.1mol•L-1的氨水,所得溶液pH及导电性变化如图.下列分析不正确的是( )| A. | b点溶液pH=5,此时酸碱恰好中和 | |
| B. | a~b点导电能力增强,说明HR为弱酸 | |
| C. | c点溶液存在c(NH4+)>c(R-)、c(OH-)>c(H+) | |
| D. | b~c任意点溶液均有c(H+)•c(OH-)=KW=1.0×10-14 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NA个Fe(OH)3胶体粒子的质量为107 g | |
| B. | 8.0 g Cu2S和CuO的混合物中含有铜原子数为0.1NA | |
| C. | 标准状况下,2.24 L Cl2溶于水中达到饱和,可得到HClO分子的数目是0.1NA | |
| D. | 1 mol Na2O2固体中含离子总数为4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
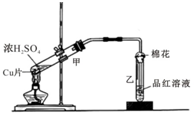 如图为浓硫酸与铜片反应的装置.请回答:
如图为浓硫酸与铜片反应的装置.请回答:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
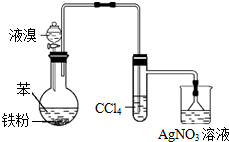
| A. | 该装置中CCl4的作用是除去产物HBr中混有的Br2蒸气 | |
| B. | 若将液溴改为浓溴水,该反应也能进行 | |
| C. | 通过AgNO3溶液中有淡黄色沉淀产生,说明由苯制溴苯的反应是取代反应 | |
| D. | 该装置中左侧长导管的作用是导气兼冷凝回流 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com