
| A. | 纤维素进入人体内会完全水解为葡萄糖从而为人体提供能量 | |
| B. | 含有食品添加剂的食物对人体均有害 | |
| C. | 硫酸铝可除去水体中的悬浮杂质并起到消毒杀菌的作用 | |
| D. | 含氮、磷元素的化合物大量排入江河湖泊中会导致水体富营养化 |
分析 A.人体能不含纤维素酶;
B.所谓食品添加剂,是指为改善食品品质和色、香、味以及为防腐、保鲜和加工工艺的需要而加入食品中的人工合成或者天然物质;
C.硫酸铝能净水,不能杀菌消毒;
D.氮和磷为植物生长的营养剂,大量排入水域后会导致水体富营养化污染.
解答 解:A.人体能不含纤维素酶,不能消化吸收纤维素,故A错误;
B.所谓食品添加剂,是指为改善食品品质和色、香、味以及为防腐、保鲜和加工工艺的需要而加入食品中的人工合成或者天然物质,有合法食品添加剂与违法食品添加剂之分,含有违法食品添加剂的食品不能食用,故B错误;
C.硫酸铝水解生成氢氧化铝胶体,具有吸水性,能够吸附水中固体杂质颗粒,所以能净水,但是不具有杀菌消毒作用,故C错误;
D.含氮、磷的化合物排放到水中会使水体出现富营养化,使某些藻类迅速繁殖,从而造成水体缺氧,使其他水生生物因缺氧而死亡,破坏生态系统,故D正确;
故选:D.
点评 本题考查了生活中常见的化学知识,为高频考点,侧重于化学与生活、生产的考查,有利于培养学生良好的科学素养,题目难度不大,注意对相关内容的积累.


 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 32gO2和O3的混合物中,所含氧原子数为2NA | |
| B. | 标准状况下,22.4LCl2与水反应,转移电子数为2NA | |
| C. | 标准状况下,3.36L辛烷中,所含碳原子数为1.5NA | |
| D. | 含1molFeCl3的饱和溶液,逐滴加入沸水中,完全形成Fe(OH)3胶体,胶粒数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 纯硫酸的摩尔质量为98 | |
| B. | 上述100mL稀硫酸中含溶质14g | |
| C. | 上述稀释过程所需要的蒸馏水为90mL | |
| D. | 质量分数为50%的硫酸物质的量浓度为7.14mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
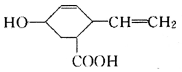
| A. | 分子式为C9H12O3,可以燃烧 | |
| B. | 能发生取代反应和聚合反应 | |
| C. | 能使酸性高锰酸钾溶液和溴的CCl4溶液褪色,褪色原理相同 | |
| D. | 分子中所有碳原子不可能共平面 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用Na2S除去废水中的Hg2+ | B. | 用热的Na2CO3溶液去油污 | ||
| C. | 利用油脂的皂化反应制造肥皂 | D. | 配制CuSO4溶液时加少量稀H2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
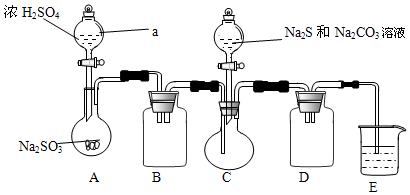
| 实验操作 | 现象 | 结论 |
| 取适量产品配成稀溶液,滴加足量BaCl2溶液 | 有白色沉淀生成 | |
| 过滤,用蒸馏水洗涤沉淀,向沉淀中加入足量稀HCl | 沉淀部分溶解,并有刺激性气味的气体产生 | 确定产品中含有Na2SO3和Na2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
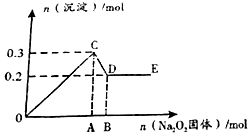 有一透明溶液,可能含有较大量的Mg2+、Fe3+、Al3+、Cu2+、Na+、SO42-、OH-中的一种或几种离子,取此溶液做下列实验.
有一透明溶液,可能含有较大量的Mg2+、Fe3+、Al3+、Cu2+、Na+、SO42-、OH-中的一种或几种离子,取此溶液做下列实验.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
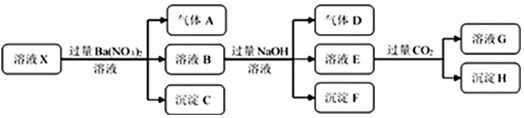
| A. | 若要确定溶液X中是否含有Fe3+,其操作为取少量原溶液于试管中,加入适量KSCN溶液,溶液变血红色,则含有Fe3+ | |
| B. | 沉淀C为BaSO4,沉淀H为BaCO3 | |
| C. | 溶液中一定含有H+、Al3+、NH4+、Fe2+、SO42-、Cl- | |
| D. | 若溶液X为100mL,产生的气体A为112mL(标况),则X中c(Fe2+)=0.05mol•L-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com