
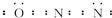 ,其分子空间构型是直线形.
,其分子空间构型是直线形.分析 (1)N2O与CO2具有相似的结构,应为直线形分子,且存在N=O键,N2O分子中氧原子只与一个氮原子相连,应为N=N=O结构;
(2)COCl2分子的结构式为 ,中心C原子形成2个单键和1个双键,共3个价层电子对,所以为sp2杂化;氯仿变质生成HCl,氯化氢能够与硝酸银反应生成氯化银沉淀;
,中心C原子形成2个单键和1个双键,共3个价层电子对,所以为sp2杂化;氯仿变质生成HCl,氯化氢能够与硝酸银反应生成氯化银沉淀;
(3)①氙为稀有气体,最外层8个电子;
②1mol氙气和3.5mol氟气于密闭容器中,在一定条件下使反应完毕,剩余有1.5mol氟气,则反应可2mol氟气,氙气为单原子分子,则白色固体为XeF4.
解答 解:(1)N2O与CO2具有相似的结构,应为直线形分子,且存在N=O键,N2O分子中氧原子只与一个氮原子相连,应为N=N=O结构,电子式: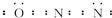 ,分子构型为直线型;
,分子构型为直线型;
故答案为: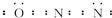 ;直线;
;直线;
(2)COCl2分子的结构式为 ,中心C原子形成2个单键和1个双键,共3个价层电子对,所以为平面三角形结构;氯仿变质生成HCl,氯化氢能够与硝酸银反应生成氯化银沉淀,所以可以用硝酸银溶液检验,故选:D;
,中心C原子形成2个单键和1个双键,共3个价层电子对,所以为平面三角形结构;氯仿变质生成HCl,氯化氢能够与硝酸银反应生成氯化银沉淀,所以可以用硝酸银溶液检验,故选:D;
故答案为:平面三角形; D;
①氙属于第五周期,氙为稀有气体,最外层8个电子,氙的外围电子排布式为 5s25p6;
1mol氙气和3.5mol氟气于密闭容器中,在一定条件下使反应完毕,剩余有1.5mol氟气,则反应可2mol氟气,氙气为单原子分子,则n(Xe):n(F)=1:4,
化学式为XeF4,
故答案为:5s25p6 XeF4.
点评 本题考查较为综合,涉及物质的结构、电子式、检验以及计算,侧重于考查综合运用化学知识的能力,题目难度不大,注意把握题给信息.


 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案科目:高中化学 来源: 题型:解答题
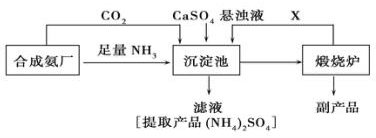
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 甲肾上腺素的分子式为:C8H10NO3 | |
| B. | 1 mol去甲肾上腺素最多能与2 mol Na发生反应 | |
| C. | 1 mol去甲肾上腺素最多能与2 mol Br2发生取代反应 | |
| D. | 去甲肾上腺素能发生加成、取代、消去和氧化反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com