
【题目】某同学用KSCN溶液和FeCl2溶液探究Fe2+的还原性时出现异常现象,实验如下:
① | ② | ③ |
|
|
|
溶液变红,约10秒后红色褪去,产生能使带火星木条复燃的气体,取褪色后溶液,滴加盐酸和BaCl2溶液,产生白色沉淀 | 溶液变红且不褪色,有能使带火星木条复燃的气体产生,产物经检验有丁达尔效应 | 溶液变红且不褪色,滴加盐酸和BaCl2溶液,无白色沉淀,产物经检验无丁达尔效应 |
下列说法错误的是
A.②中红色溶液中含有Fe(OH)3胶体
B.实验②中发生的氧化还原反应只有两种
C.对比①②,可以判定酸性条件下H2O2可以氧化SCN-
D.③中发生的氧化还原反应为:4Fe2++O2+4H+=4Fe3++2H2O
【答案】B
【解析】
A项、由实验②的实验现象可知,产物经检验有丁达尔效应,说明酸性条件下H2O2将Fe2+氧化为Fe3+,Fe3+水解形成红色Fe(OH)3胶体,故A正确;
B项、由实验②的实验现象可知,实验中存在的反应有酸性条件下H2O2将Fe2+氧化为Fe3+、在Fe3+做催化剂作用下,双氧水分解生成水和氧气,由实验①的实验现象可知,实验中还存在的反应还有酸性条件下H2O2可以氧化部分SCN-,三个反应均属于氧化还原反应,故B错误;
C项、对比实验①②的实验现象可知,酸性条件下H2O2可以氧化SCN-,生成的硫酸根与氯化钡溶液反应生成白色沉淀,故C正确;
D项、由实验③的实验现象可知,酸性条件下,O2将Fe2+氧化为Fe3+,反应的离子方程式为4Fe2++O2+4H+=4Fe3++2H2O,故D正确;
故选B。


 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案科目:高中化学 来源: 题型:
【题目】某容积固定的密闭容器中发生可逆反应:A (g)+2B (g)![]() C (s)+D (g),能说明反应已达到平衡状态的事实是
C (s)+D (g),能说明反应已达到平衡状态的事实是
A. 容器内A、B、C、D四者共存 B. νA(正)=2νB(逆)
C. 容器内各种物质的浓度不再改变 D. νA(正)=νC(逆)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下0.1mol/L①CH3COOH、②NaOH、③CH3COONa,下列叙述正确的是( )
A.①中[CH3COOH]>[CH3COO-]>[H+]>[OH-]
B.①②等体积混合后,醋酸根离子浓度小于③的二分之一
C.①③等体积混合以后,溶液呈酸性,则(Na+)>(CH3COO-)>(H+)
D.①②等体积混合以后,水的电离程度比①③等体积混合的电离程度小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】绿矾是重要的工业原料,在实验室里探究在高温下绿矾的分解产物。
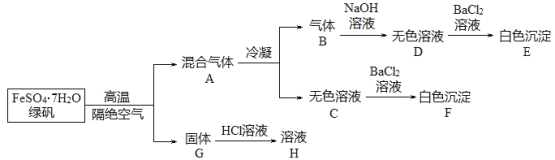
取27.8g绿矾晶体,按上述流程进行实验,测得白色沉淀E和F的质量分别为10.85g和11.65g。
(1)通过计算,写出绿矾隔绝空气高温分解的反应方程式:______。
(2)实验室检验溶液H中金属阳离子的步骤和现象:______。
(3)白色沉淀E在空气中放置一段时间后称量,发现质量大于10.85g,用化学方程式来解释这个现象:______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A是用于制造汽车发动机的耐高温陶瓷材料,A由两种元素组成,取2.05g A在纯氧中充分反应,得到2.55g固体E和一种气体G。一定条件下,A还存在如下图所示的物质转化关系,其中C、F、K是无色无味的气体单质,D、H是固体单质。反应②常用于汽车尾气的处理。
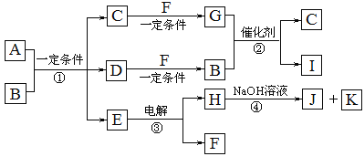
(1)C的电子式_________。
(2)A中所含元素形成的二种简单离子的半径_______大于_______。(填离子符号)
(3)反应②的化学方程式_______________________。
(4)写出反应④的离子方程式_______________________。
(5)A在潮湿的空气里不稳定,产生一种刺激性气味的气体,写出反应的化学方程式_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】恒容密闭容器中发生反应:2NO2(g)![]() 2NO(g)+O2(g)(NO2红棕色气体,NO无色气体),下列状态中不能表明该反应达到平衡状态的有( )
2NO(g)+O2(g)(NO2红棕色气体,NO无色气体),下列状态中不能表明该反应达到平衡状态的有( )
A.混合气体的颜色不再改变的状态
B.单位时间内生成nmolO2的同时生成2nmolNO2
C.混合气体的密度不再改变的状态
D.混合气体的平均相对分子质量不再改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究表明N2O与CO在Fe+作用下发生反应的能量变化及反应历程如图所示,下列说法错误的是

A. 反应总过程△H<0
B. Fe+使反应的活化能减小
C. 总反应若在2L的密闭容器中进行,温度越高反应速率一定越快
D. Fe++N2O→FeO++N2、FeO++CO→Fe++CO2两步反应均为放热及应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下进行下列实验,根据实验操作和现象所得到的结论正确的是( )
选项 | 实验操作和现象 | 结论 |
A | 向苯酚钠溶液中滴加NaHSO3溶液,溶液变浑浊 | 苯酚酸性弱于H2SO3酸性 |
B | 向AgNO3溶液中逐滴加入浓度均为0.05 mol·L-1的NaI、NaCl混合溶液,有黄色沉淀生成 | Ksp(AgCl)>Ksp(AgI) |
C | 向FeCl3溶液中加入Cu粉,Cu粉溶解 | Cu的还原性大于Fe |
D | 向盛有H2O2溶液的试管中滴几滴酸化的FeCl2溶液,溶液变成棕黄色,一段时间后,溶液中有气泡出现 | 铁离子催化H2O2的分解 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ. 由中科院等离子体物理研究所自主研制的全超导托卡马克实验装置(俗称“人造太阳”)正在接受技术升级。人造太阳是利用氘、氚核聚变反应释放巨大能量原理而实现的。下列说法正确的是________。
A.氕、氘、氚三种元素在周期表中的位置不同
B.20 g D2O含有的中子数为6.02×1024个
C.在隔绝空气和高温下LiCl与金属钠反应可获得金属锂
Ⅱ. 部分元素在周期表中的位置如下:

请回答下列问题:
(1)元素C在周期表中的位置为________。
(2)判断E和F对应的简单氢化物沸点高低,并解释原因____________。
(3)用电子式表示F的氢化物的形成过程:___________。
Ⅲ.溴及其化合物广泛用于医药、塑料阻燃剂等,苦卤提溴的工业流程如下:
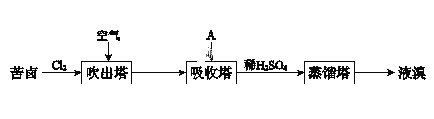
(1)结合元素周期律解释Cl的非金属性强于Br的原因:_______________。
(2)吸收塔中,A吸收了Br2后的溶液中含有Br和BrO3,则A是________(填序号)。
A.NaCl溶液 B.Na2CO3溶液 C.SO2气体
(3)从吸收塔出来的溶液中加入稀H2SO4得到Br2的离子方程式是______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com